В статье рассмотрены составляющие метаболического стресса, определяющие гипертрофию скелетных мышц: увеличение рекрутирования мышечных волокон; повышенное производство гормонов; изменение производства миокинов; производство активных форм кислорода; набухание мышечных волокон.

Schoenfeld B.J. Potential Mechanisms for a Role of Metabolic Stress in Hypertrophic Adaptations to Resistance Training // Sports Med. 2013. Vol. 43. P. 179–194.
Шёнфельд Бред
ПОТЕНЦИАЛЬНЫЕ МЕХАНИЗМЫ РОЛИ МЕТАБОЛИЧЕСКОГО СТРЕССА В ГИПЕРТРОФИЧЕСКОЙ АДАПТАЦИИ К ТРЕНИРОВКАМ C ОТЯГОЩЕНИЯМИ
Аннотация
Хорошо известно, что регулярные тренировки с отягощением могут способствовать мышечной гипертрофии. Преобладающее количество исследований показывает, что механический стресс является основным стимулом для этой адаптивной реакции. Исследования показывают, что только механический стресс может инициировать анаболические сигналы. Учитывая доминирующую роль механического стресса в мышечном росте, возникает вопрос о том, могут ли могут ли другие факторы усиливать посттренировочный гипертрофический ответ. Некоторые исследователи предположили, что метаболический стресс, вызванный физической нагрузкой, может на самом деле оказывать такой анаболический эффект, а некоторые даже предположили, что накопление метаболитов может быть более важным, чем большие усилия для оптимизации мышечного роста. Метаболический стресс, возникающий в результате традиционных тренировок с отягощением, проявляется в результате упражнений, которые основываются на анаэробном гликолизе для производства аденозинтрифосфата (АТФ). Это, в свою очередь, вызывает последующее накопление метаболитов, в частности, лактата и ионов водорода (H+). Острая мышечная гипоксия, связанная с такими методами тренировки, может еще больше усилить накопление метаболитов. Таким образом, целью данной статьи является обзор новых исследований, предполагающих роль метаболического стресса, вызванного тренировками, с целью максимальной гипертрофии мышц. Также предполагается рассмотреть потенциальные механизмы, с помощью которых эти гипертрофические адаптации могут быть достигнуты. Эти механизмы включают в себя: усиление вовлечения мышечных волокон в работу, повышенное производство гормонов, изменения в локальных миокинах, повышенное производство реактивных форм кислорода и набухание мышечных волокон. Даны рекомендации относительно потенциальных областей будущих исследований по данному вопросу.
1. Введение
Хорошо известно, что регулярные тренировки с отягощением могут способствовать увеличению мышечной гипертрофии. В настоящее время преобладающее количество исследований указывает на то, что механический стресс является основным стимулом для этой адаптивной реакции. Эти результаты были описаны в основополагающей работе Goldberg A.L. et al. [1], которые сообщили, что развитие повышенной силы является критическим событием в инициировании компенсаторного мышечного роста. Впоследствии многочисленные исследования подтвердили этот вывод как in vitro (в пробирке), ex vivo (вне живого), так и in vivo (внутри живого) [2-6].
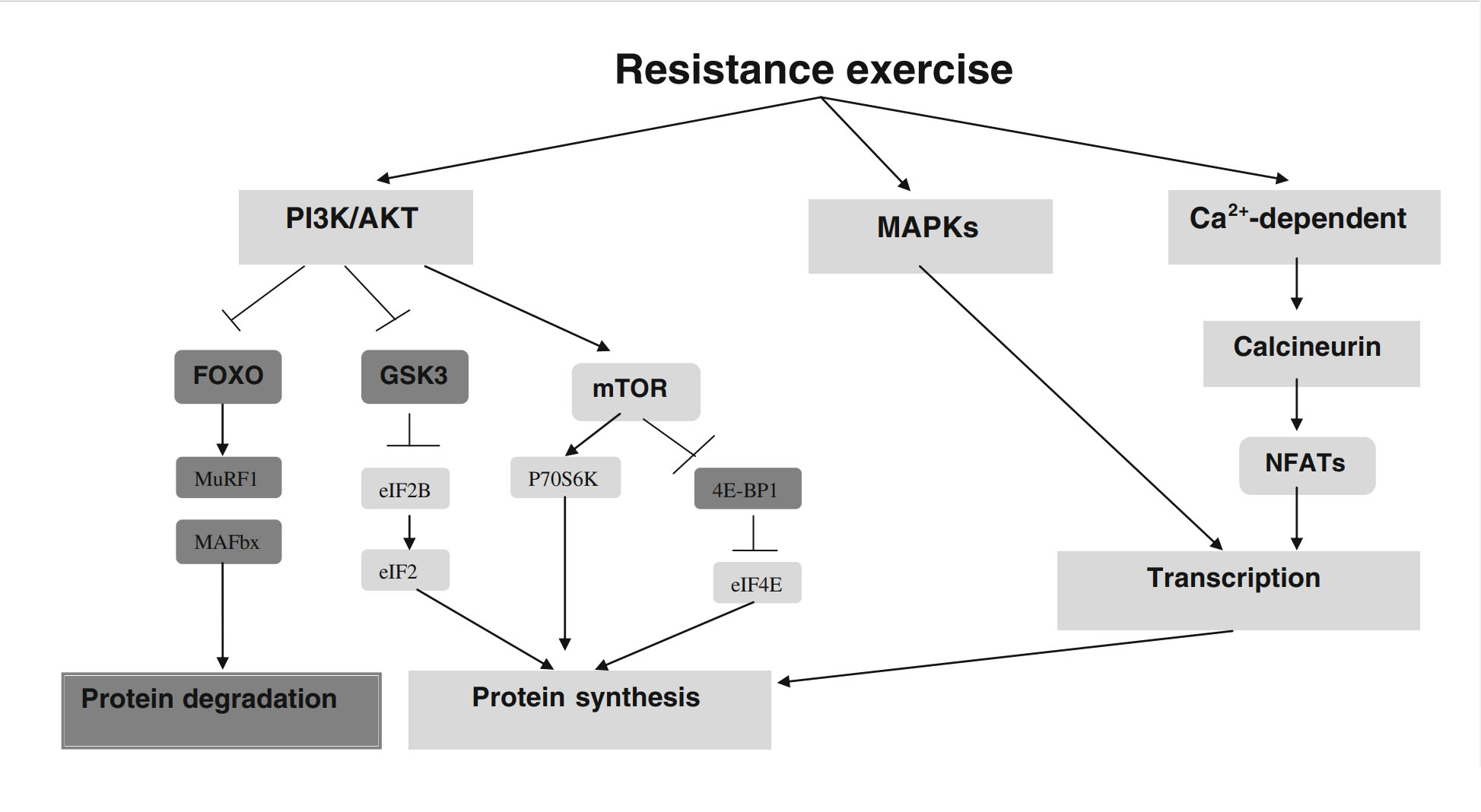
Современная теория предполагает, что силы, связанные с физическими упражнениями с отягощениями, нарушают целостность скелетной мышцы, вызывая механохимически-трансдуцированные молекулярные и клеточные реакции в миофибриллах и клетках-сателлитах [7]. Вызванная физическими упражнениями гипертрофия мышц облегчается сложным каскадом анаболических и катаболических сигнальных путей. При этом эффекты механостимуляции молекулярно передаются на нижележащие мишени, которые сдвигают баланс мышечных белков в пользу синтеза, а не деградации. Многие анаболические сигнальные пути участвуют в увеличении мышечной массы, вызванной физическими упражнениями, в то время как другие непосредственно опосредуют клеточные процессы, которые влияют на трансляцию мессенджерной РНК (мРНК) и, следовательно, на гипертрофию мышц [8]. Пути, которые были определены как особенно важные для мышечного анаболизма, включают mTOR, митоген-активируемую протеинкиназу (MAPK) и различные кальций-зависимые пути. Хотя эти пути могут пересекаться на ключевых этапах регуляции, есть доказательства того, что они скорее синергичны, чем дублируют друг друга [9]. Однако точные механизмы и взаимодействие между ними еще предстоит выяснить. Полное обсуждение этой темы выходит за рамки данной статьи статью, а заинтересованных читателей отсылаем к обзорам Bassel-Duby и Olson [10], Miyazaki и Esser [11] и Glass [12]. На рисунке 1 представлена упрощенная блок-схема различных сигнальных каскадов и их отношение к анаболическим и катаболическим процессам.
Было показано, что механический стресс непосредственно стимулирует mTOR [13], возможно, через активацию внеклеточной регулируемой киназы/комплекса туберозного склероза 2 (ERK/TSC2) [6]. Предполагается, что эти действия опосредуются через синтез липидного второго мессенджера фосфатидной кислоты (ФК) фосфолипазой D [13, 14]. Имеются также доказательства того, что ФК может фосфорилировать нижележащий анаболический трансляционный регулятор p70S6 киназа (p70S6k) независимо от mTOR [15], представляя собой еще один потенциальный путь, по которому механические стимулы могут непосредственно влиять на синтез мышечного белка.
Учитывая доминирующую роль механического стресса в мышечном росте, возникает вопрос о том, могут ли другие факторы усиливать посттренировочный гипертрофический ответ. Несколько исследователей предположили, что вызванный физической нагрузкой метаболический стресс может на самом деле оказывать такое воздействие [16-18], а некоторые даже предположили, что накопление метаболитов может быть более важным, чем развитие высокой силы мышцей, для оптимизации мышечного роста [19]. Другие исследователи, однако, оспаривают подобные утверждения [20]. Поэтому целью данной статьи является обзор нового массива исследований, предполагающих роль индуцированного тренировками метаболического стресса в максимальном развитии скелетных мышц, а также представить потенциальные механизмы, с помощью которых могут происходить эти гипертрофические адаптации. Для проведения данного обзора был проведен поиск англоязычной поиск литературы в PubMed, EBSCO и Google. Базы данных Scholar были проведены для всех временных периодов вплоть до апреля 2012 года. В качестве условий поиска использовались комбинации следующих ключевых слов использовались в качестве поисковых терминов: «метаболический стресс», «метаболиты накопление», «накопление метаболитов», «тренировка с отягощением», «поднятие веса», «бодибилдинг», «пауэрлифтинг», «анаболический гормон», «KAATSU», «упражнения с окклюзией», «упражнения с ограничением кровотока» и «набухание клеток». Списки ссылок на статьи, полученные в результате поиска, затем были проверены на наличие дополнительных статей, имеющих отношение к данной теме. Учитывая широкий охват данного обзора, был выбран описательный подход как наилучший способ передачи соответствующей информации, а критерии включения были основаны на применимости к конкретной области обсуждения.
2. Доказательства гипертрофического эффекта метаболизма стресса
Метаболический стресс в результате физических упражнений проявляется как результат накопления метаболитов, особенно лактата, фосфорных остатков и ионов водорода (H+) [21, 22], а острая мышечная гипоксия, связанная с тренировкой с отягощением, может служить для дальнейшего усиления метаболизма и, следовательно, стимулировать гипертрофические адаптации [7, 23]. Можно предположить, что гипоксия может оказывать прямое влияние на накопление сократительных белков и тем самым способствовать гипертрофическому стимулу, хотя это еще изучено недостаточно. Другие метаболиты, имеющие возможное отношение к анаболизму, относятся к кальцию и различным электролитам. Подтверждение потенциальной гипертрофирующей роли метаболического стресса, вызванного физическими упражнениями, можно отметить эмпирически, изучив режим тренировок умеренной интенсивности, принятые большинством бодибилдеров, которые предназначены для усиления метаболического роста за счет более высокой интенсивности тренировок [24, 25]. Типичные тренировки, ориентированные на гипертрофию мышц в бодибилдинге, включают в себя выполнение нескольких сетов по 6-12 повторений в каждом сете с относительно короткими межсетовыми интервалами отдыха [26]. Было установлено, что такие тренировки вызывают значительно больший метаболический стресс, чем более высокоинтенсивные режимы, обычно используемые пауэрлифтерами [27-29]. Тем не менее, несмотря на тренировки с пониженной интенсивностью, бодибилдеры обычно демонстрируют экстремальные уровни мускулатуры, по крайней мере, такие же, если не более значительные, чем у пауэрлифтеров [25, 30]. Действительно, в ряде исследований сообщалось о большей гипертрофии мышц в результате тренировок умеренной интенсивности типа бодибилдинга по сравнению с высокоинтенсивными тренировками в стиле пауэрлифтинга [31-33], хотя эти результаты не совпадают во всех исследованиях при уравнивании нагрузки по объему [34]. Следует отметить, что как бодибилдеры и пауэрлифтеры, как известно, используют анаболические стероиды и другие фармакологические средства, что может нарушить способность делать твердые выводы по данной теме.
Повышенный метаболический ответ, связанный с тренировками умеренной интенсивности (*60-80% от 1-го повторного максимума [1ПМ]), может быть, по крайней мере, частично, приписано увеличению энергетического вклада от быстрого гликолиза, который приводит к периферическому, а не центральному утомлению (т.е. утомлению, связанному с метаболическими и/или биохимическими изменениями, а не снижением нейронных импульсов) [35]. Уровень лактата в мышцах 91 ммоль/кг сухого веса был зарегистрирован после выполнения 1 сета из 12 повторений до отказа (общее время под напряжение среднее ± стандартное отклонение [SD] 37 ± 3 с) и эти значения увеличились до 118 ммоль/кг после трех сетов [36]. Это контрастирует с высокоинтенсивным протоколам (90% 1ПМ), где энергия обеспечивается в основном за счет фосфагенной системы и, следовательно, приводит к минимальному метаболизму. Более того, доставка кислорода к мышцам нарушается при умеренной интенсивности из-за постоянного сжатия артериального и венозного кровотока в течение длительного периода времени, что приводит к острой гипоксии [37]. В сочетании эти факторы вызывают быстрое накопление метаболитов в скелетных мышцах, а также снижению уровня внутримышечного pH [38].
Экспериментальные данные, показывающие, что метаболический стресс вносит свой вклад в гипертрофический ответ, можно проиллюстрировать на примере тренировочных исследований KAATSU, в которых упражнения с отягощениями сочетаются с ограничением кровотока. KAATSU-тренировки проводятся при низкой интенсивности (обычно 40% от 1ПМ) при использовании манжеты, чтобы вызвать мышечную ишемию. Большое количество доказательств показывает, что этот тип тренировки стимулирует анаболические сигналы и синтез белка [39] и приводит к выраженной гипертрофии скелетных мышц [40], несмотря на то, что интенсивность ниже 60% 1ПМ часто считается слишком низкой, чтобы вызвать значительную гипертрофическую реакцию [34, 41].
Накопление метаболитов значительно повышено в KAATSU [42], что позволяет предположить связь между метаболическим стрессом и гипертрофией мышц. Интересно, что Abe et al. [43] обнаружили, что ходьба с манжетами с давлением приводит к значительному увеличению площади поперечного сечения мышц бедра (CSA) у студентов (4-7%) в течение всего лишь трех недель. Такие низкоинтенсивные аэробные тренировки обычно не ассоциируются с гипертрофией мышц у здоровых молодых людей, что указывает на то, что факторы, отличные от механического стресса были ответственны за гипертрофическую адаптацию.
Дальнейшие доказательства связи между метаболическим стрессом и мышечной гипертрофией могут быть получены из исследований, в которых тренировки проводились в гипоксической среде. Kon M. et al. [44] показали, что выполнение нескольких комплексов низкоинтенсивных упражнений (50% 1ПМ) с умеренными интервалами отдыха (1 мин.) при дыхании 13% кислородом значительно увеличивало накопление метаболитов, определяемое по уровню лактата в крови, по сравнению с аналогичными упражнениями в нормоксических условиях. Эти результаты были подтверждены Nishimura et al. [45], которые обнаружили, что выполнение типичного протокола, ведущего к гипертрофии мышц (4 сета по 10 повторений при 70% 1ПМ) в условиях острой гипоксии привело к значительному большему увеличению CSA мышц локтевых сгибателей и разгибателей по сравнению с аналогичным тренингом в нормоксических условиях.
3. Потенциальные механизмы действия
Механизмы, которые, как предполагается, опосредуют гипертрофическую адаптацию при метаболическом стрессе, вызванном физическими упражнениями, включают в себя повышенную активацию мышечных волокон, повышенное системное производство гормонов, изменения в локальных миокинах, повышенное производство реактивных форм кислорода (ROS) и набухание мышечных волокон [45-48]. В следующем разделе мы обсудим каждый из этих предполагаемых механизмов и их потенциальную роль в гипертрофическом ответе на тренировки с отягощением. На рисунке 2 представлен обзор того, как эти факторы могут сочетаться для усиления мышечного роста.
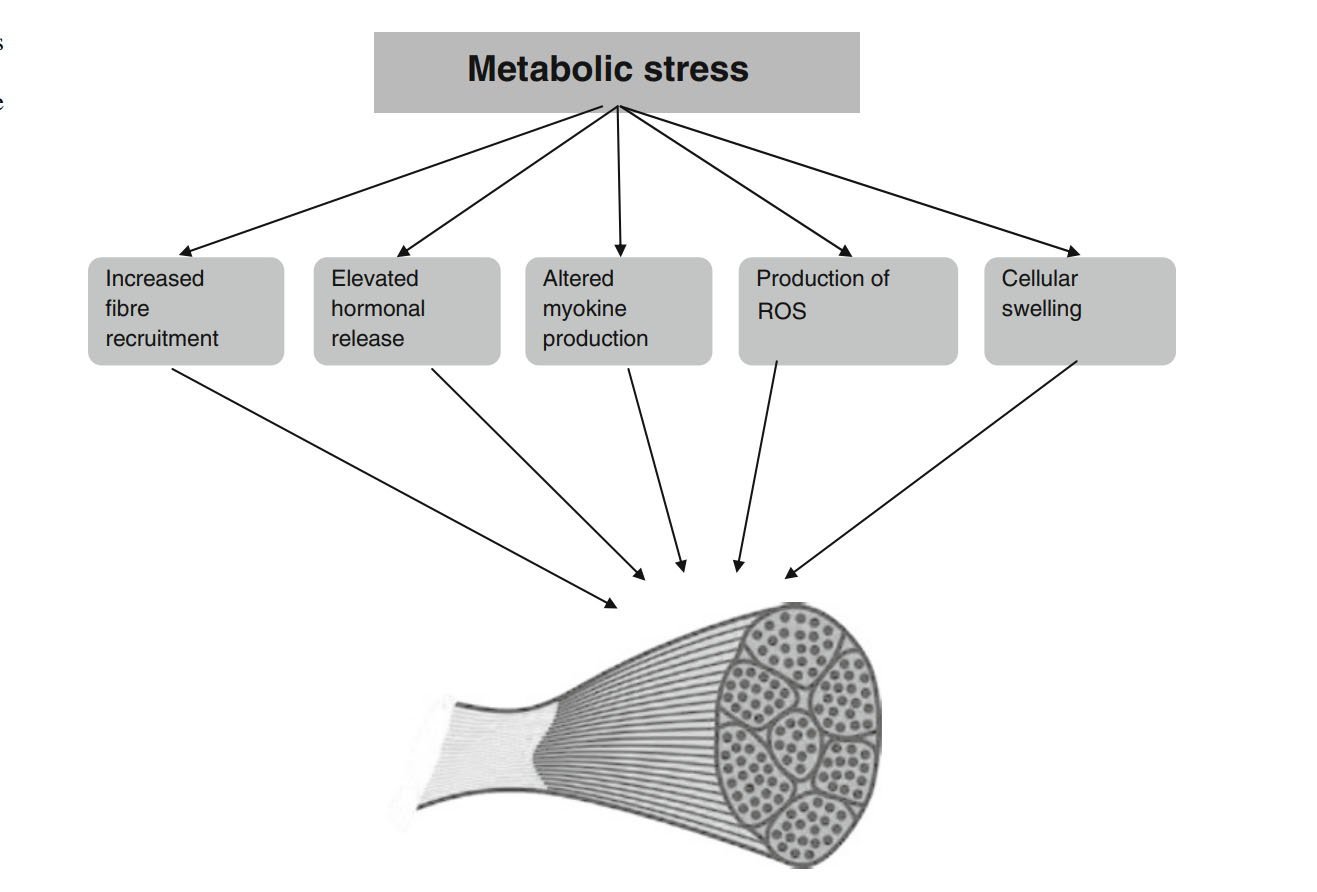
4. Рекрутирование мышечных волокон
Принцип размера диктует, что с увеличением интенсивности тренировки для поддержания мышечного сокращения постепенно привлекаются более крупные двигательные единицы (ДЕ), содержащие быстрые мышечные волокна (FT) [49]. Учитывая, что мышечные волокна (МВ) должны быть рекрутированы для того, чтобы реагировать и адаптироваться к физическим нагрузкам с отягощениями [50], необходимо тренироваться на очень высоких уровня интенсивности для максимальной гипертрофии мышц. Однако существуют убедительные доказательства того, что метаболический стресс на самом деле увеличивает рекрутирование более высокопороговых двигательных единиц даже в условиях низкой нагрузки. Многочисленные исследования показали, что пороги рекрутирования ДЕ снижаются во время продолжительных субмаксимальных упражнений с увеличением уровня утомления [51-53]. Таким образом большее количество волокон типа FT задействуется по мере того, как наступает критическая точка мышечного утомления. Кроме того, исследования с использованием электромиографии (ЭМГ) [48, 54], истощения гликогена [55] и расщепления органического фосфата [22, 38], показали усиленное привлечение FT-волокон при тренировках KAATSU. Поэтому некоторые исследователи предположили, что это основной механизм, с помощью которого такие упражнения вызывают гипертрофические адаптации [56, 57].
Точные механизмы, посредством которых метаболический стресс усиливает рекрутирование FT-волокон, еще предстоит выяснить. Существует предположение, что эффект опосредован накоплением ионов водорода (H+), которое подавляет сократительную способность скелетных мышц и тем самым способствуя привлечению дополнительных высокопороговых двигательных единиц [54, 58, 59]. Кроме того, некоторые исследователи предположили, что гипоксия вызывает активацию FT-волокон в попытке поддержать необходимый уровня генерации силы [60, 61]. Другая возможность заключается в том, что выработка свободных радикалов, которая увеличивается при выполнении упражнений с метаболическими нагрузками, вызывает повышенное привлечение FT-волокон, ускоряя наступление утомления [59]. Учитывая сложность мышечного утомления, вызванного физической нагрузкой, кажется правдоподобным, что комбинация этих факторов и, возможно, других, в конечном счете, участвует в этом процессе. Хотя увеличение рекрутирования волокон представляет собой убедительное обоснование метаболически индуцированной мышечной гипертрофии, связанной с тренировками с отягощением, остается под вопросом является ли это единственным механизмом, ответственным за такие адаптации. Используя модель, в которой изучалось расщепление органического фосфата с помощью магнитно-резонансной спектроскопии, Suga T. et al. [22] обнаружили, что рекрутирование FT-волокон произошло только у 31% испытуемых, выполнявших окклюзионную тренировку при 20% 1ПМ, по сравнению с 70% испытуемых, тренировавшихся при 65% 1ПМ. Учитывая, что этот низкий уровень интенсивности (20% 1ПМ) был показан для увеличения гипертрофии мышц в сочетании с ограничением кровотока в такой же или большей степени, как и высокоинтенсивные тренировки [62, 63], поэтому представляется вероятным, что другие факторы, также вносят свой вклад в гипертрофический эффект метаболического стресса, вызванного физической нагрузкой. Для дополнительной поддержки этому выводу, исследования ЭМГ показали, что упражнения, выполняемые при 80% 1ПМ, вызывают значительно большую мышечную активность по сравнению с упражнениями с ограничением кровотока при 20% 1ПМ, что указывает на снижение рекрутирования при более низкой интенсивности [64].
5. Системная гормональная продукция
Другая популярная теория, предложенная для объяснения гипертрофических механизмов, связанных с метаболическим стрессом, заключается в том, что накопление метаболитов увеличивает концентрацию гормонов, тем самым усиливая анаболическую среду и последующее накопление мышечных белков [46, 65]. Теоретически, высокие уровни циркулирующих гормонов увеличивают вероятность взаимодействия с рецепторами [66], что может иметь имеет особое гипертрофическое значение в послетренировочный период, когда мышцы готовы к анаболизму. Некоторые исследователи предполагают, что эти острые гормональные подъемы, вызванные тренировкой, более важны для роста и ремоделирования мышц, чем хронические изменения концентрации гормонов в состоянии покоя [67]. Метаболически индуцированные скачки инсулиноподобного фактора роста (ИФР-1), тестостерона и гормона роста (ГР), в частности, оказывают положительное влияние на посттренировочный синтез мышечного белка. Ниже приводится обзор каждого из этих гормонов и их потенциальной гипертрофической значимости для упражнений с отягощением, которые способствуют существенным изменениям внутриклеточной метаболической среды.
5.1. ИФР-1
ИФР-1 – это гомологичный пептидный гормон, который обладает как митогенным и анаболическим действием на скелетные мышцы [68]. Была установлена четкая причинно-следственная связь между ИФР-1 и мышечной гипертрофией [68], и некоторые исследователи утверждают, что ИФР-1 является основным физиологическим регулятором мышечной массы [69]. Анаболические эффекты ИФР-1, по-видимому, усиливаются в ответ на механическую нагрузку [70], а увеличение количества белка под воздействием ИФР-1 пропорционально увеличению мышечной силы после тренировок с отягощением [71]. Однако, исследования показывают, что функциональный рецептор ИФР-1 не является обязательным для компенсаторного роста мышц [3].
Были идентифицированы три различные изоформы ИФР-1: системные формы ИФР-1Еа и ИФР-1Еb, а также сплайс-вариант, ИФР-1Ec. Хотя каждая из этих изоформ экспрессируется в мышечной ткани [72], только ИФР-1Ec, по-видимому, локально активируется механическими сигналами, и поэтому он был назван механофактором роста (МФР) [70]. Несмотря на то, что МФР функционирует в аутокринном/ паракринном режиме и, таким образом, не является настоящим гормоном, он, тем не менее, будет обсуждаться в этом разделе, учитывая его тесную связь с другими изоформами ИФР-1.
Хотя печень является основным местом эндокринной выработки ИФР-1, другие непеченочные ткани, включая мышцы, также экспрессируют системные изоформы. Фактически, во время интенсивных физических нагрузок большая часть ИФР-1Еа поступает из работающих мышц, а не из печени, и большая часть циркулирующего ИФР-1 в конечном итоге поглощается мускулатурой [73]. Влияние системно вырабатываемого ИФР-1 на мышечную гипертрофию не совсем ясно, и есть некоторые сомнения в том, играет ли он значительную роль в посттренировочном мышечном росте белка [74]. Вполне возможно, что основная гипертрофическая роль этих изоформ заключается в стимулировании слияния клеток-сателлитов с существующими мышечными волокнами, тем самым облегчая донорство миоядер и помогая поддерживать оптимальное соотношение ДНК и белка в мышечной ткани [7, 75]. Поскольку отношение количества ядер мышцы (миоядер) к массе мышечного волокна во время гипертрофии остается неизменным, считается, что добавление новых миоядер за счет клеток-сателлитов необходимо для реализации долгосрочного увеличения мышечной массы [76]. Это согласуется с концепцией миоядерного домена, которая предполагает, что миоядра регулируют производство мРНК для конечного объема саркоплазмы и любое увеличение размера мышечного волокна должно сопровождаться пропорциональным увеличением количества миоядер [77]. Значимость миоядерного домена остается спорным и те, кто заинтересованные в подробном обсуждении этой темы, отсылаются к статьям O’ Connor и Pavlath [78] и McCarthy и Esser [79].
В отличие от этого, локально экспрессируемый МФР, как полагают, является изоформой, в основном ответственной за компенсаторную гипертрофию мышц [80]. Из-за его быстрой экспрессии после механической нагрузки, МФР, как полагают, помогает «запустить гипертрофический ответ после тренировки и облегчает локальное восстановлению поврежденной ткани» [73]. МФР осуществляет сигнализацию через многочисленные анаболические каскады, включая фосфатидилинозитол 3-киназу-белковую киназу В-млекопитающую мишень рапамицина (PI3). рапамицина (PI3K-Akt-mTOR) [81], MAPK-ERK 1/2 [82], и различные кальций-зависимые пути [9], тем самым непосредственно опосредуя синтез мышечных белков. Недавний кластерный анализ post hoc, проведенный Bamman MM et al. [83], показал, что МФР дифференцированно экспрессируется в разных кластерах, при этом у экстремально реагирующих на тренировки с отягощением наблюдается устойчивое увеличение, а у нереагирующих наблюдалась лишь незначительная тенденция к повышению. Эти результаты убедительно свидетельствуют о том, что острое, преходящее повышение экспрессии гена МФР являются важными сигналами для гипертрофической адаптации в ответ на механические нагрузки. Более того, в то время как системно вырабатываемый ИФР-1Ea опосредует слияние клеток-сателлитов [7, 75], локально выраженный МФР как полагают, активирует клетки-сателлиты и опосредует их пролиферацию и дифференцировку [84, 85]. Таким образом, по-видимому, существует синергизм между местными и системными изоформами для оптимизации содержания миоядер и таким образом, способствуя долгосрочному увеличению мышечной массы. Полное обсуждение роли различных изоформ ИФР-1 выходит за рамки данной статьи. Тех, кто заинтересован в дальнейшем исследовании этой темы, мы рекомендуем обратиться к недавним обзорам от Velloso и Harridge [74] и Philippou et al. [86].
Выполнение тренировок гипертрофированного типа, которые создают интенсивное наращивание метаболизма, как было установлено, приводит к значительно большему повышению уровня циркулирующего ИФР-1 по сравнению с высокоинтенсивными протоколами, которые вызывают минимальное накопление метаболитов [28, 29, 87], хотя эти результаты не были единообразными во всех исследованиях [88]. Более того, некоторые [89-91], но не все [92] исследования KAATSU показали повышенный пост-тренировочный подъем ИФР-1 после окклюзионных упражнений, что говорит о метаболически индуцированном влиянии на гормон. Причина этих расхождений не ясна и может быть функцией методологических различий между протоколами. Более того, вышеупомянутые исследования в основном изучали системное производство ИФР-1, что затрудняет оценку потенциальных гипертрофических последствий, если такая связь действительно существует.
5.2. Тестостерон
Тестостерон – это холестериновый гормон, синтезируемый и секретируется в основном клетками Лейдига яичек посредством гипоталамо-гипофизарно-гонадной оси, с небольшим количеством, получаемым из яичников и надпочечников [93]. Анаболический эффект тестостерона на мышечную ткань неоспоримо проявляется [94, 95]. Например, тестостерон увеличивает синтез мышечного белка и снижает протеолиз [96, 97]. Эти эффекты вызываются его связыванием с внутриклеточным андрогенным рецептором, который, в свою очередь, перемещается в ядро, где этот комплекс вызывает транскрипцию генов [98]. В дополнение к этим прямым анаболическим функциям, тестостерон также оказывает косвенные гипертрофические эффекты, которые включают потенцирование высвобождение других анаболических гормонов, таких как ГР [66] и ИФР-1/МФР [99], а также опосредованную активацию и пролиферацию клеток-сателлитов [100].
Существует предположение, что резкое повышение тестостерона после тренировки может напрямую стимулировать анаболизм путем
увеличения скорости синтеза белка и подавляя протеолиз [93]. Это согласуется с данными, показывающими значительную корреляцию между вызванным тренировкой повышением тестостерона и увеличением мышечной CSA [101]. Результаты кажутся более выраженными у атлетов по сравнению со спортсменами на выносливость и сидячими людьми [102], что позволяет предположить, что посттренировочный тестостерон может играть большую роль по мере накопления опыта тренировок с отягощением [103]. Тем не менее, причинно-следственная связь между острой выработкой тестостерона и гипертрофией мышц еще не установлена, и есть убедительные доказательства того, что повышение тестостерона после тренировки не является необходимым для компенсаторного роста мышц [104].
Попытки определить влияние метаболического стресса на тестостерон были в основном неубедительными. Хотя несколько исследований показали, что ориентированные на гипертрофию мышц программы тренировок с отягощениями, вызывают большее посттренировочное повышение тестостерона по сравнению с тренировками [93, 105-108], которые не обнаружили существенных различий [28, 38, 109]. Более того, тренировки KAATSU в целом не продемонстрировали значительного повышения тестостерона после тренировки, несмотря на высокие уровни метаболитов [91, 109, 110], что ставит вопрос о том, играет ли этот гормон роль в метаболическом стрессе, вызванном гипертрофическим ответом. Следует отметить, что пол, возраст, опыт тренировок и состояние питания могут влиять на высвобождение тестостерона [67], и эти факторы могут объяснять противоречивые результаты, наблюдаемые в исследованиях на сегодняшний день. Необходимо дальнейшее изучение этой темы чтобы можно было прийти к более определенному выводу.
5.3. Гормон роста
Гормон роста (ГР) – это суперсемейство полипептидных гормонов, которые действуют как перераспределяющие агенты, вызывающие метаболизм жира в направлении мобилизации триглицеридов, а также стимулирует клеточное поглощение и включение аминокислот в различные белки, включая мышечные [111]. Однако, несмотря на свое название, прямое гипертрофическое действие ГР на мышечный белок, по-видимому, незначительное, а эффекты, по-видимому, ограничивается синтезом неконтрактильной ткани (т.е. коллагена) [112]. Считается, что ГР в первую очередь осуществляет мышечный анаболизм путем потенцирования высвобождения ИФР-1 [75], хотя некоторые исследователи оспаривают эту теорию и постулируют, что гипертрофические эффекты ГР и ИФР-1 на самом деле являются аддитивными [113]. Существуют данные о том, что введение рекомбинантного ГР заметно повышает уровень мРНК МГФ в сочетании с физическими упражнениями только пожилых людей [70], однако это не наблюдается у здоровых молодых взрослых людей [114]. ГР также, по-видимому, оказывает разрешающий или, возможно, даже синергический эффект на тестостерон-опосредованный синтез белка [98]. Однако неясно, какое влияние, если таковое вообще имеется, оказывают преходящие эндогенные посттренировочные скачки ГР на уровни МГФ или тестостерона в это время. Действие суперсемейства ГР весьма разнообразны и сложны, и их полное обсуждение выходит за рамки данной статьи. Тех, кто заинтересован в дальнейшем чтении могут обратиться к недавним обзорам Ehrnborg C, Rosen T. [115] и Kraemer et al. [116].
Преобладающее количество исследований подтверждает сильную корреляцию между метаболическим стрессом, вызванным физической нагрузкой, и повышенной гипофизарной секрецией ГР [23, 46-48, 90, 105, 106]. Абсолютная величина этих гормональных повышений является значительной. Fujita S. Et al. [91] обнаружили, что KAATSU увеличивает уровень ГР после тренировки в 10 раз выше по сравнению с низкоинтенсивной тренировкой без ограничения кровотока, в то время как Takarada Y. et al. [48] сообщили о 290-кратном повышении по сравнению с исходного уровня. Повышение уровня ГР после тренировки предположительно опосредовано повышенным накоплением лактата и/или H+ в крови [47, 106]. Снижение рН, связанное с накоплением метаболитов, также может потенцировать ГР, что способствует анаболизму тканей [118]. Анаболическая роль острой выработки ГР, в частности, была отвергнута в основном на основании исследований, показывающих, что экзогенное введение рекомбинантного ГР не приводит к большему увеличению накопления мышечного белка [119-121]. Хотя это может быть правдой, следует отметить, что экзогенные инъекции не имитируют ответ in vivo на индуцированную физическими упражнениями секрецию ГР ни по времени, ни по величине. Анаболическая среда активизируется после тренировки, и вполне возможно, что возможно, что большие скачки ГР наблюдаются после тренировки с отягощением, который может в 300 раз превышать исходный уровень [48], может способствовать регенерации организма. [48], а также ремоделированию после травмы мышц. Кроме того, рекомбинантный ГР состоит исключительно из 22-кДа изоформы [115], в то время как более 100 молекулярных изоформ ГР вырабатывается эндогенно [122]. Широкий спектр этих изоформ достигает пика при завершении тренировки с большей пропорциональной концентрацией не-22-кД изоформ [115]. Супрафизиологические дозы рекомбинантного ГР фактически препятствуют посттренировочной стимуляции этих альтернативных изоформ [115], потенциально затушевывая гипертрофические эффекты. Оказывают ли эти факторы значительное влияние на мышечную адаптацию, на данный момент не ясно и требует дальнейшего изучения.
West D.W. et al. [123] обнаружили, что преходящие гормональные всплески не оказывают влияния на синтез мышечного белка после тренировки у молодых мужчин по сравнению с протоколом, в котором уровень гормонов был низким. Более того, фосфорилирование p70S6k было одинаковым между группами, что указывает на то, что анаболические сигналы также не были затронуты послетренировочным повышением уровня гормонов после тренировки. Важно отметить, однако, что синтез белка, измеренный в ответ на острую тренировку, не всегда коррелирует с хронической регуляцией миогенных сигналов [124] и не всегда предсказывает долгосрочный гипертрофический ответ на регулярные тренировки [76]. Таким образом, хотя эти результаты интригуют, их практическое значение ограничено.
Прямые исследования, оценивающие влияние острого анаболического гормонального производства на гипертрофию мышц, были противоречивыми. Madarame H. et al. [125] обнаружили, что выполнение окклюзионной тренировки для мышц нижней части тела после одностороннего упражнения на руки привело к значительному увеличению площади поперечного сечения (CSA) сгибателей локтя по сравнению с идентичной тренировкой рук в сочетании с неокклюзионной тренировкой нижней части тела. Хотя различия в уровнях ГР не достигли статистической значимости, авторы утверждают, что это было вызвано вероятно, из-за недостаточной мощности исследования. Принимая во внимание, что аналогичные протоколы показали значительный посттренировочный гормональный рост [23, 46-48, 90, 106], результаты, таким образом, позволяют предположить, что системные факторы могли играть определенную роль в адаптивной реакции. Также интересно отметить, что что в нетренированной руке не наблюдалось изменений в CSA мышц, что указывает на то, что острое системное гормональное повышение не влияет на размер мышц в нетренированной руке в отсутствие механического стресса.
West D.W. et al. [126] использовали модель «в пределах одного человека» для изучения роли острого гормонального повышения на мышечную гипертрофию, используя для этого используя традиционный протокол упражнений с отягощением. Двенадцать нетренированных мужчин (возраст средний ± SD 21,8 ± 1,2 года) тренировали сгибатели локтя в отдельные дни в двух различных гормональных условиях: в условиях низкого уровня гормонов, когда одна рука выполняла только упражнение на разгибание, и в условиях высокого уровня гормонов, когда противоположная рука выполняла то же упражнение на разгибание руки после чего сразу же выполнялось упражнение на сопротивление ног, разработанное для того, чтобы вызвать значительное увеличение циркулирующих гормонов. Через 15 недель не было обнаружено различий между группами в обхвате мышц, определенном с помощью магнитно-резонансной томографии, несмотря на значительно большее повышение уровня циркулирующих ИФР-1, ГР и тестостерона в группе с высоким содержанием гормонов после физических упражнений.
В недавнем исследовании Ronnestad B.R. et al. [127] схожее с исследованием West D.W. et al. [126], за исключением того, что тренировка ног выполнялась до тренировки рук в группе с высоким содержанием гормонов. В отличие от исследования West D.W. et al. [126], испытуемые в группе с высоким уровнем гормонов продемонстрировали значительно большее увеличение CSA мышц сгибателей локтя, что говорит о том, что повышенный уровень гормонов был ответственен за гипертрофию мышц. Интересно, что различия были характерны для отдельных областей локтевых сгибателей, причем увеличение CSA мышцы наблюдалось только в двух средних отделах, где мышечный обхват был наибольшим.
Принимая во внимание противоречивые данные, преждевременно делать окончательные выводы о том, играет ли роль в мышечной гипертрофии анаболический гормональный ответ после тренировки, связанный с метаболическим стрессом. Что из проведенных исследований кажется очевидным, так если такая роль действительно существует на самом деле, общая величина эффекта будет довольно скромной. Однако даже скромное увеличение мышечной гипертрофии потенциально может быть значимым для определенных групп населения, особенно бодибилдеров и силовых атлетов. Можно предположить, что резкое повышение гормонального уровня может оказывать большее влияние на активность клеток-сателлитов, а не на скорость синтеза белка после тренировки, тем самым влияя на долгосрочные, а не краткосрочные гипертрофические адаптации. Если это так, то анаболические эффекты этих гормональных скачков могут быть ограничены генетическими различиями в предтренировочном уровне доступности клеток-сателлитов и последующей способности человека расширить доступный пул клеток-сателлитов [77]. Наконец, исследования на тренированных людях по данному вопросу отсутствуют, поэтому предстоит выяснить, реагируют ли люди с предыдущим опытом тренировок по-другому реагируют на острую тренировку, вызванную физической нагрузкой по сравнению с нетренированными субъектами.
6. Локальные миокины
Тренировка с физической нагрузкой приводит к синтезу различных цитокинов и других пептидов в скелетных мышцах (т.н. миокины), и появляющаяся совокупность доказательств указывает на то, что эти местные факторы могут вносить значительный вклад в гипертрофическую адаптацию [128-130]. Многие из этих агентов могут оказывать влияние аутокринным/паракринным образом, чтобы вызвать уникальные эффекты на адаптацию скелетных мышц, и тренировки с отягощением, по-видимому, усиливают их реакцию [131]. Существует предположение, что метаболический стресс может опосредовать мышечную гипертрофию путем повышения уровня анаболических миокинов и/или понижения уровня катаболических миокинов.
Интерлейкин (IL)-6 является миокином ранней стадии, который, как предполагается, может влияет на опосредованную клетками-сателлитами аккрецию (увеличение количества) миоядерных клеток [130], и было предположено, что индуцированный физической нагрузкой метаболический стресс может стимулировать его выработку [132]. Несмотря на кажущееся теоретическое обоснование, однако, доказательства в поддержку этого утверждения отсутствуют. Takarada Y et al. [48] обнаружили, что упражнение с ограничением кровотока в разгибателях голени приводит к постепенному увеличению уровня IL-6, при этом уровни сохраняются на повышенном уровне через 24 часа после тренировки по сравнению с контролем. Однако общий размер эффекта был небольшим, уровни достигали лишь одной четвертой от тех, о которых сообщалось при эксцентрических упражнениях более высокой интенсивности. Fujita T. et al. [133] сообщили об увеличении на 2,4% CSA мышц бедра после 6 дней KAATSU, несмотря на то, что уровень IL-6 оставался неизменным в течение всего периода тренировок. Аналогично, исследования, проведенные Abe T. et al. [134] и Fry C.S. et al. [39] не смогли обнаружить изменения в уровнях IL-6 после окклюзионной тренировки. Эти результаты заставляют усомниться в том, что IL-6 на самом деле является механизмом, с помощью которого метаболический стресс вызывает гипертрофию мышц. Существуют некоторые данные, позволяющие предположить, что метаболический стресс может оказывать большее влияние на компенсаторную гипертрофию мышц уменьшая местные катаболические факторы, в отличие от увеличения факторов, направленных на рост. Учитывая, что мышечный рост представляет собой динамический баланс между синтезом и распадом белка, снижение распада белка в конечном итоге приводит к увеличению накопления белка. Исследования потенциальных медиаторов в основном сосредоточены на миостатине, являющемся членом суперсемейства трансформирующего фактора роста-3, который действует как негативный регулятор мышечного роста [135]. Kawada и Ishii [136] обнаружили, что уровень миостатина значительно снизился в плантарной мышце крыс линии Вистар после упражнений с ограниченным кровотоком по сравнению с контрольной группой. В отличие от этого, исследование на людях, проведенное Drummond MJ et al. [92] сообщили об отсутствии различий в миостатине экспрессии генов между тренировками KAATSU и низкоинтенсивными упражнениями без ограничения кровотока через 3 часа после тренировки. Интересно, что Manini TM et al. [137] обнаружили, что, хотя KAATSU не снижает уровень миостатина, он значительно снижает уровень различных протеолитических транскриптов (forkhead box O3A [FOXO3A], Atrogin-1 и muscle ring finger-1 [MuRF-1]) через 8 часов после тренировки по сравнению с контрольной группой, которая выполняла тренировки низкой интенсивности без отягощений. Недавно Laurentino GC et al. [63] исследовали влияние KAATSU на хронический уровень миостатина у физически активных мужчин. После 8 недель тренировок KAATSU вызвал значительное хроническое снижение экспрессии генов миостатина на 45%, в то время как низкоинтенсивные тренировки без ограничения кровотока показали лишь незначительное снижение уровня миостатина. Учитывая разрозненные данные, трудно сделать однозначные выводы о том, влияет ли метаболический стресс на гипертрофию мышц путем изменения выработки миокинов. Важно отметить, что в литературе было выявлено множество дополнительных миокинов (включая IL-1, IL-7, IL-8, IL-10, IL-13, IL-15, фактор роста фибробластов, лейкемия ингибирующий фактор лейкемии, фактор некроза опухоли и др.) и влияние метаболического стресса на эти миокины еще предстоит изучить. Более того, не удалось найти ни одного исследования, в которых бы напрямую сравнивали посттренировочные уровни миокинов между традиционными тренировками, ориентированными на гипертрофию мышц, и высокоинтенсивными тренировками, ориентированными на силу. Эта тема должна стать основной для будущих исследований.
7. Реактивные виды кислорода
ROS (реактивные формы кислорода) представляют собой интригующий потенциальный механизм, с помощью которого метаболический стресс может опосредовать мышечную гипертрофию. Термин ROS включает в себя как кислородные радикалы (т.е. супероксидные, гидроксильные, пероксильные и гидропероксильные радикалы) и нерадикальные окислители (например, перекись водорода и хлорноватистую кислоту) [138]. Полное обсуждение источников производства ROS, индуцированного сокращением, выходит за рамки данной статьи, однако различают ROS, образующиеся хронически в состоянии покоя, и ROS, образующиеся во время тренировки. В нормальных физиологических условиях ROS в основном генерируются митохондриальной электронно-транспортной цепью и окислением полиненасыщенных жиров, и на их производство значительно влияют экологический стресс и старение [138].
Во время физической нагрузки сокращающиеся мышцы являются основным источником острого производства ROS, причем уровень возрастания зависит от типа и интенсивности тренировки [139]. Для получения дополнительной информации по этому вопросу заинтересованный читатель может обратиться к недавним исследованиям. Мощные антиоксиданты, демонстрируют увеличение вызванного физической нагрузкой мышечного роста, что указывает на ROS-опосредованный гипертрофический ответ через окислительно-восстановительные сигнальные пути [149]. Хотя механизмы действия не были полностью выяснены, исследования показали, что ROS может влиять на мышечную гипертрофию через усиление сигнализации MAPK. Kefaloyianni et al. [150] показали, что обработка C2 миобластов вариантом ROS увеличивает активацию MAPK, причем реакция различных подсемейств MAPK (ERK 1/2, c-Jun N-terminal kinase [JNK] и p38-MAPK) различаются по времени. В сердечных миоцитах ROS может регулировать фосфолипазу D и, таким образом, потенциально опосредовать синтез белка синтез белка через активацию PA [151]. Влияет ли ROS на этот путь в скелетных мышцах, пока не установлено. Существуют также доказательства того, что лечение антиоксидантами значительно снижает ИФР-1 индуцированное фосфорилирование рецептора ИФР-1 в миоцитах С2C12 [151], обработанных ROS, предполагая, что ROS имеет критическую функцию в биологическом действии ИФР-1 [152].
Исследования, подтверждающие гипертрофирующую роль ROS в действиях, вызывающих метаболический стресс, остаются спекулятивными и в основном получены на основе предполагаемых данных. Митохондрии в FT волокнах обладают уникальными свойствами, которые способствуют более высоким уровням активности ROS по сравнению с медленно сокращающимися волокнами [140]. Учитывая, что тренировки гипертрофического типа, связанные с метаболическим стрессом, предположительно вовлекают митохондрии в большей степени, чем высокоинтенсивные тренировки, представляется разумным разумно заключить, что такие тренировки будут генерировать больше ROS. Более того, гипоксия и последующая реперфузия увеличивает производство ROS [153, 154]. Поскольку большее время под напряжением, связанное с гипертрофией мышц обязательно будет связано с увеличением ишемического ответа по сравнению с высокоинтенсивными тренировками, то вполне логично, что будут вырабатываются более высокие уровни ROS. Являются ли эти различия в производстве ROS достаточными для развития гипертрофического ответа, на данный момент неизвестно и требуют дальнейшего изучения. Прямой эффект метаболического стресса, вызванного физической нагрузкой, на ROS не был хорошо изучен. Goldfarb AH et al. [155] показали, что уровень карбонила белка в плазме и соотношение глутатиона в крови — оба маркера окислительного стресса, были значительно выше при выполнении упражнений гипертрофического типа (3 сета при *70% 1ПМ) по сравнению с низкоинтенсивным режимом с ограничением кровотока (3 сета при *30% 1ПМ), что говорит о том, что повреждение мышц играет доминирующую роль в генерировании ROS. Подтверждение этой гипотезы было продемонстрировано Takarada Y et al. [48], которые не обнаружили изменений в посттренировочном уровне перекиси липидов после выполнения разгибания ног в приседе в сочетании с окклюзией сосудов, при этом повреждение мышц было минимальным. Интересным, но относительно неизученным аспектом исследований в этой области является оксид азота (NO), один из вариантов ROS. Производство NO было связано с компенсаторной мышечной гипертрофией [156, 157], и есть доказательства того, что он опосредует увеличение активации и пролиферации клеток-сателлитов [158], возможно, через синтез фактора роста гепатоцитов [159]. Kawada и Ishii [136] продемонстрировали, что венозная окклюзия задних конечностей у крыс линии Вистар привела к увеличению экспрессии NO синтазы-1 (NOS-1), фермента, который катализирует увеличение фактора роста – фермента, катализирующего производство NO из L-аргинина. Однако, несмотря на то, что уровни NO показали тенденцию к увеличению через 2 недели после операции (p = 0,10), результаты не достигли статистической значимости, предположительно из-за большого межсубъектного разброса. Подтверждающие исследования на людях в настоящее время отсутствуют.
ROS также может косвенно влиять на гипертрофию мышц путем транскрипции высококонсервативных стрессовых белков, называемых белками теплового шока (HSPs). В нормальных физиологических условиях HSPs действуют как белки-шапероны, облегчая сворачивание новых пептидных цепей и транслокацию белков [160]. Когда организм подвергается стрессу, однако, считается, что HSPs выполняют защитную роль, которая включает ограничение окислительного повреждения, вызванного ROS [161], и некоторые исследователи предполагают, что они могут играть роль в компенсаторной мышечной гипертрофии [136, 162]. Было идентифицировано несколько HSPs, каждый из которых назван в соответствии с их молекулярной массой в килодальтонах (например, HSP27, HSP60, HSP70, HSP72 и т.д.). Следует отметить, что в дополнение к ROS-опосредованной транскрипции, HSPs также индуцируются гипоксией, ацидозом, и ишемией-реперфузией [163] – все это побочные продукты тренировок с отягощением, связанные с высоким уровнем метаболического стресса. Kawada S, Ishii N. [136] обнаружили, что HSP72 был значительно повышен в плантарной мышце крыс после двух недель окклюзии сосудов. Эти данные были связаны со значительным увеличением мышечной гипертрофии, что позволило исследователям предположить, что HSP72 может способствовать развитию мышц после тренировки. И наоборот, Fry CS et al. [39] не обнаружили различий в общем содержании белка HSP70 после выполнения упражнений с ограниченным кровотоком при 20% 1ПМ у пожилых мужчин.
Кроме того, недавнее исследование, проведенное Paulsen G et al. [164] показало, что объем тренировки (один сет против трех не влияет на цитозольные или цитоскелетные уровни HSP27 и HSP70 ни в латеральном мышечном слое, ни в трапециевидной мышце после 11 недель прогрессивных тренировок гипертрофического типа (7-10 RM). Учитывая, что более высокие объемы тренировки обязательно приведут к большему накоплению метаболитов – это свидетельствует против наличия дозовой зависимости между метаболическим стрессом и HSPs. Возможно, наиболее важным является то, что транскрипция HSP в результате упражнений с отягощениями, скорее всего, обусловлена структурными и функциональными повреждениями мышц, а не повышенной продукцией ROS [165]. Сочетание этих результатов заставляет усомниться в том являются ли HSP на самом деле значительным гипертрофическим механизмом, связанным с метаболизмом, вызванным физическими упражнениями.
8. Набухание клеток (набухание мышечных волокон)
Один из более новых механизмов, который может быть вовлечен в гипертрофический ответ на метаболический стресс, включает в себя увеличение внутриклеточной гидратации. Это явление, известное как набухание мышечных волокон, как полагают, служит физиологическим регулятором клеточной функции [166, 167]. Многочисленные исследования показали, что опосредованное гидратацией набухание клеток приводит к увеличению синтеза белка и уменьшению протеолиза в целом ряде различных типов клеток, которые включают гепатоциты, остеоциты, клетки молочной железы и мышечные волокна [168]. В отношении скелетных мышц была выдвинута теория о том, что стимул, связанный с набуханием мышечных волокон, может вызвать пролиферацию клеток-сателлитов и способствовать их слиянию с гипертрофирующимся миофибриллами [169], тем самым усиливая потенциальные долгосрочные гипертрофические адаптации. Механизмы, лежащие в основе индуцированного набуханием мышечных волокон анаболизма, еще предстоит полностью выяснить. Предполагается, что повышенное давление на цитоскелет и/или клеточной мембраны воспринимается как угроза клеточной целостности, что заставляет мышечное волокно инициировать сигнальный ответ, который в конечном итоге приводит к укреплению ее ультраструктуры [24, 170]. Существуют доказательства того, что сигнализация осуществляется через интегрин-ассоциированные объемные осмосенсоры внутри клеток [171]. Сенсоры, в свою очередь, активируют анаболические протеин-киназные пути трансдукции, возможно, опосредованные аутокринными эффектами факторов роста [172, 173]. Исследования показывают, что анаболические функции осуществляются в mTOR-независимым образом [174], и есть предположение, что модули MAPK могут быть первичным медиатором анаболизма, индуцированного набуханием [175, 176].
На сегодняшний день существует мало исследований, непосредственно изучающих, усиливает ли клеточная гидратация в результате накопления метаболитов, вызванного физической нагрузкой, рост мышц. Однако можно привести убедительные аргументы в пользу того, что это происходит. Было показано, что тренировки с отягощением вызывают изменения внутриклеточного и внеклеточного водного баланса [177], степень которого зависит от типа упражнения и интенсивности тренировки. Набухание мышечных волокон максимально увеличивается при выполнении упражнений, которые в значительной степени зависят от гликолиза, в результате чего накапливается лактат, действующий как основной вклад в осмотические изменения в скелетных мышцах [178, 179]. Как было показано, что внутримышечное накопление лактата запускает механизмы регуляции объема, и эти эффекты могут быть усилены кислой средой связанная с индуцированным физической нагрузкой накоплением метаболитов [168]. Хотя это и предположительно, объём отёка может быть усилен реактивной гиперемией в результате сдавливания кровеносных сосудов во время тренировки. FT-волокна особенно чувствительны к осмотическим изменениям, предположительно связанным с высокой концентрацией водных транспортными каналами, называемыми аквапорин-4 (AQP4). AQP4 как было показано, сильно экспрессируется в сарколемме гликолитических и окислительно-гликолитических волокон FT млекопитающих. волокон, облегчая приток жидкости в клетку [179]. Учитывая, что волокна FT наиболее чувствительны к гипертрофии [180], можно предположить, что клеточная гидратация влияет на гипертрофический ответ во время тренировок с отягощением, включающей сильный гликолитический компонент, путем производства благоприятное воздействие на чистый белковый баланс и, таким образом, усиливая аккрецию мышечного белка. Следовательно, «мышечный насос», к которому часто стремятся бодибилдеры, может на самом деле в конечном счете, способствовать росту. Поэтому тренировочные программы, ориентированные на гипертрофию мышц, могут быть полезны, если максимально использовать это явление.
Хотя гипотеза набухания мышечных волокон является интригующей, недавнее исследование, проведенное Gundermann DM et al. [181] предоставляет доказательства обратного. В исследовании сравнивались низкоинтенсивные тренировки с отягощением, при которых гиперемия моделировалась с помощью фармакологических сосудорасширяющих средств, чтобы уменьшить кровоснабжение. Результаты показали, что упражнения с окклюзией приводили к увеличению фракционной синтетической скорости смешанных мышц на 49%, а также к значительному повышению фосфорилирования mTOR, S6K1 и ERK1/2, в то время как у тех, кто выполнял упражнения, дополненные фармакологической вазодилатацией (расширение сосудов), не показали изменений ни в одной из этих переменных. Исследование было ограничено тем фактом, что исследователи не смогли не смогли точно воспроизвести незамедлительно (в течение первых 10 мин) посттренировочную гиперемическую реакцию, что затрудняет определение того, играет ли начальный сигнал от повышенной гидратации определенную роль в посттренировочном протеине синтеза. Кроме того, распад белка не измерялся, а ослабление протеолиза, как полагают, является основным средством, с помощью которого клеточная гидратация опосредует мышечную гипертрофию.
Возможно, что метаболический стресс может привести к долгосрочному гипертрофированному приросту в результате увеличения запасов гликогена, опосредованного хроническим набуханием клеток. Хронические, последовательные тренировки на сопротивление с использованием диапазона повторений, который полагается на анаэробный гликолиз для получения энергии, значительно увеличивает запас гликогена [182]. Исследования также показывают, что культуристы демонстрируют на 50% большее содержание внутримышечного гликогена по сравнению с не спортсменами, что свидетельствует об адаптивной реакции на тренировки гипертрофированного типа [21]. Учитывая, что гликоген привлекает три грамма воды на каждый грамм гликогена [183], то увеличение запасов гликогена может опосредовать благоприятный мышечный белковый баланс с течением времени через повышенную клеточную гидратацию мышечных волокон, тем самым усиливая долгосрочный гипертрофический прирост. Эта теория остается непроверенной и требует дальнейшего изучения.
9. Заключение
В целом несмотря на то, что механический стресс, несомненно, является основным движущим стимулом в посттренировочном мышечном росте, существуют убедительные доказательства того, что метаболический стресс также может способствовать гипертрофической адаптации. Что неясно, так это является ли метаболический стресс дополнительным к механически обусловленным сигнализациям или, возможно, является избыточным при условии достижения определенного уровня интенсивности. Проблема современных исследований заключается в том, что механический и метаболический стресс происходят в тандеме, поэтому что затрудняет выделение эффектов одного из них из другого. Это может потенциально может привести к неправильной интерпретации метаболических факторов как причинно-следственной связи.
Кроме того, механизмы, посредством которых метаболический стресс влияет на компенсаторную гипертрофию мышц, еще предстоит полностью исследовать. Хотя рекрутирование мышц, в значительной степени влияет на гипертрофию мышц, сомнительно, что только рекрутинг отвечает за всю величину связанных с ростом прироста. Скорее, объединенная интеграция множества местных и системных факторов, вероятно, способствует развитию мышц прямым и/или благоприятным образом [184]. В дополнение к механизмам, рассмотренным в данном обзоре, возможно, что другие еще не установленные факторы также могут и необходимы для более глубокого изучения этой темы. Современная теория предполагает, что определенный порог механического стресса необходим для стимулирования мышечного роста, который, предположительно, находится в диапазоне приблизительно 60-65% 1RM [41]. В поддержку этой рекомендации можно на основании исследования Campos GER et al. [34], которые обнаружили, что что скорректированные по объему тренировки высокой (3-5 ПМ) и умеренной интенсивности (9-11 ПM) способствовали значительному увеличению в мышечной CSA бедра, в то время как тренировки низкой интенсивности (20-28 ПM) не способствовали.
Однако последние исследования противоречат этим выводам. Tanimoto M et al. [185] продемонстрировали, что тренировки с 50% от 1ПМ с медленным движением и тонической генерацией силы (3 с для эксцентрического и концентрического без фазы расслабления) показали сопоставимое увеличение размеров мышц по сравнению с тренировками при 80% 1ПМ с традиционным способом (1 с для концентрических и эксцентрических действий). Результаты были объяснены увеличением метаболического стресса, связанного с протоколом более низкой интенсивности. Совсем недавно Mitchell CJ et al. [186] показали, что 10 недель тренировок разгибателей ног с интенсивностью 30% от 1ПМ привели к аналогичному гипертрофическому ответу, что и тренировки с интенсивностью с интенсивностью 80% 1ПМ, хотя результаты были несопоставимы из-за значительно большого объема в группе с низкой интенсивностью. В отличие от этого, Holm L et al. [187] сообщили, что протокол умеренной интенсивности (70% 1ПМ) привел к трехкратному увеличению мышечной гипертрофии по сравнению с выровненным по объему протоколом низкой интенсивности (15,5% 1ПМ) в течение 12-недельного тренировочного периода. Расхождения между этими исследованиями, скорее всего, связаны с методологией и требуют дальнейшего изучения. Следует отметить, что гипертрофия мышц, связанная с тренировками более низкой интенсивности, в значительной степени зависит от тренировок «до отказа». Это, вероятно, связано с тем, что утомляющие сеты необходимы при более низкой интенсивности, чтобы вызвать значительный метаболический стресс и тем самым усилить соответствующие механизмы, ответственные за рост мышц. Будущие исследования должны быть направлены на выяснение точных механизмов, посредством которых метаболический стресс опосредует компенсаторный рост мышц, включая вопрос о том, играет ли сама гипоксия прямую роль в этом процессе. Кроме того, следует попытаться выяснить интенсивность оптимальной гипертрофирующей нагрузки на основе взаимосвязи «сила-выносливость», и определить точную роль, которую метаболический стресс играет в этом процессе. Особое внимание должно быть сосредоточено на том, существует ли зависимость «доза-ответ» между метаболическим стрессом и мышечной гипертрофией, и если да, то существует ли верхний порог, за которым такие преимущества выходят на плато и/или результаты ухудшаются. Учитывая большое влияние возраста, пола и генетики на мышечную адаптацию, вполне вероятно, что любой такой порог будет варьировать в зависимости от индивидуальных различий. Например, пожилой бегун-марафонец с высокой долей волокон типа I в мышцах бедра будет, по-видимому, иметь иной пороговый ответ, чем молодой спринтер, у которого преобладают волокна II типа. Эти вопросы требуют дальнейшего изучения. Потенциальным фактором, является то, что индуцированный физической нагрузкой метаболический стресс обычно происходит в сочетании с повреждением мышц во время упражнений с отягощениями, ориентированных на гипертрофию мышц. Учитывая, что повреждения мышц как полагают, играют роль в посттренировочном росте мышц [188], это может изменить результаты и, следовательно, должно быть учтено при планировании исследования, поэтому это необходимо учитывать при разработке дизайна исследования. Кроме того, исследования на сегодняшний день в основном ограничиваются использованием нетренированных испытуемых, что ограничивает возможность обобщения результатов на тренированные группы населения. Поэтому исследователи должны стремиться проводить будущие исследования на атлетах, имеющих по крайней мере год или более лет целенаправленных тренировок с отягощением. Более глубокое понимание этих факторов в конечном итоге улучшит нашу способность разрабатывать программы, которые максимизируют гипертрофические адаптации, основанной на потребностях, способностях и генетики конкретного человека.
References
- Goldberg AL, Etlinger JD, Goldspink DF, et al. Mechanism of work-induced hypertrophy of skeletal muscle. Med Sci Sports. 1975 Fall;7(3):185–98.
- Witkowski S, Lovering RM, Spangenburg EE. High-frequency electrically stimulated skeletal muscle contractions increase p70s6k phosphorylation independent of known IGF-I sensitive signaling pathways. FEBS Lett. 2010;584(13):2891–5.
- Spangenburg EE, Le Roith D, Ward CW, et al. A functional insulin-like growth factor receptor is not necessary for loadinduced skeletal muscle hypertrophy. J Physiol. 2008;586(1): 283–91.
- Hornberger TA, Stuppard R, Conley KE, et al. Mechanical stimuli regulate rapamycin-sensitive signalling by a phosphoinositide 3-kinase-, protein kinase B- and growth factor-independent mechanism. Biochem J. 2004;380(Pt 3):795–804.
- Vandenburgh H, Kaufman S. In vitro model for stretch-induced hypertrophy of skeletal muscle. Science. 1979;203(4377):265–8.
- Miyazaki M, McCarthy JJ, Fedele MJ, et al. Early activation of mTORC1 signalling in response to mechanical overload is independent of phosphoinositide 3-kinase/Akt signalling. J Physiol. 2011;589(Pt 7):1831–46.
- Toigo M, Boutellier U. New fundamental resistance exercise determinants of molecular and cellular muscle adaptations. Eur J Appl Physiol. 2006;97(6):643–63.
- Mayhew DL, Hornberger TA, Lincoln HC, et al. Eukaryotic initiation factor 2B epsilon induces cap-dependent translation and skeletal muscle hypertrophy. J Physiol. 2011;589(Pt 12): 3023–37.
- Tidball JG. Mechanical signal transduction in skeletal muscle growth and adaptation. J Appl Physiol. 2005;98(5):1900–8.
- Bassel-Duby R, Olson EN. Signaling pathways in skeletal muscle remodeling. Annu Rev Biochem. 2006;75:19–37.
- Miyazaki M, Esser KA. Cellular mechanisms regulating protein synthesis and skeletal muscle hypertrophy in animals. J Appl Physiol. 2009;106(4):1367–73.
- Glass DJ. Skeletal muscle hypertrophy and atrophy signaling pathways. Int J Biochem Cell Biol. 2005;37(10):1974–84.
- Hornberger TA, Chu WK, Mak YW, et al. The role of phospholipase D and phosphatidic acid in the mechanical activation of mTOR signaling in skeletal muscle. Proc Natl Acad Sci USA. 2006;103(12):4741–6.
- O’Neil TK, Duffy LR, Frey JW, et al. The role of phosphoinositide 3-kinase and phosphatidic acid in the regulation of mammalian target of rapamycin following eccentric contractions. J Physiol. 2009;587(Pt 14):3691–701.
- Lehman N, Ledford B, Di Fulvio M, et al. Phospholipase D2-derived phosphatidic acid binds to and activates ribosomal p70 S6 kinase independently of mTOR. FASEB J. 2007;21(4): 1075–87.
- Rooney KJ, Herbert RD, Balnave RJ. Fatigue contributes to the strength training stimulus. Med Sci Sports Exerc. 1994;26(9): 1160–4.
- Schott J, McCully K, Rutherford OM. The role of metabolites in strength training. II. Short versus long isometric contractions. Eur J Appl Physiol Occup Physiol. 1995;71(4):337–41.
- Smith RC, Rutherford OM. The role of metabolites in strength training. I. A comparison of eccentric and concentric contractions. Eur J Appl Physiol Occup Physiol. 1995;71(4):332–6.
- Shinohara M, Kouzaki M, Yoshihisa T, et al. Efficacy of tourniquet ischemia for strength training with low resistance. Eur J Appl Physiol Occup Physiol. 1998;77(1–2):189–91.
- Folland JP, Irish CS, Roberts JC, et al. Fatigue is not a necessary stimulus for strength gains during resistance training. Br J Sports Med. 2002;36(5):370–3.
- Tesch PA, Colliander EB, Kaiser P. Muscle metabolism during intense, heavy-resistance exercise. Eur J Appl Physiol Occup Physiol. 1986;55(4):362–6.
- Suga T, Okita K, Morita N, et al. Intramuscular metabolism during low-intensity resistance exercise with blood flow restriction. J Appl Physiol. 2009;106(4):1119–24.
- Pierce JR, Clark BC, Ploutz-Snyder LL, et al. Growth hormone and muscle function responses to skeletal muscle ischemia. J Appl Physiol. 2006;101(6):1588–95.
- Schoenfeld BJ. The mechanisms of muscle hypertrophy and their application to resistance training. J Strength Cond Res. 2010;24(10):2857–72.
- Fry AC. The role of resistance exercise intensity on muscle fibre adaptations. Sports Med. 2004;34(10):663–79.
- Lambert CP, Flynn MG. Fatigue during high-intensity intermittent exercise: application to bodybuilding. Sports Med. 2002;32(8):511–22.
- Kraemer WJ, Fleck SJ, Dziados JE, et al. Changes in hormonal concentrations after different heavy-resistance exercise protocols in women. J Appl Physiol. 1993;75(2):594–604. 28. Kraemer WJ, Marchitelli L, Gordon SE, et al. Hormonal and growth factor responses to heavy resistance exercise protocols. J Appl Physiol. 1990;69(4):1442–50.
- Kraemer WJ, Gordon SE, Fleck SJ, et al. Endogenous anabolic hormonal and growth factor responses to heavy resistance exercise in males and females. Int J Sports Med. 1991;12(2): 228–35.
- Katch VL, Katch FI, Moffatt R, et al. Muscular development and lean body weight in body builders and weight lifters. Med Sci Sports Exerc. 1980;12(5):340–4.
- Schmidtbleicher D, Buehrle M. Neuronal adaptation and increase of cross-sectional area studying different strength training methods. In: Jonsson GB, editor. Biomechanics X-B volume 6-B. Champaign: Human Kinetics; 1987. p. 615–20.
- Choi J, Takahashi H, Itai Y. The difference between effects of ‘power-up type’ and ‘bulk-up type’ strength training exercises: with special reference to muscle cross-sectional area. Jpn J Phys Fitness Sports Med. 1998;47(1):119–29.
- Masuda K, Choi JY, Shimojo H, et al. Maintenance of myoglobin concentration in human skeletal muscle after heavy resistance training. Eur J Appl Physiol Occup Physiol. 1999; 79(4):347–52.
- Campos GER, Luecke TJ, Wendeln HK, et al. Muscular adaptations in response to three different resistance-training regimens: specificity of repetition maximum training zones. Eur J Appl Physiol. 2002;88(1–2):50–60.
- Robbins DW, Goodale TL, Docherty D, et al. The effects of load and training pattern on acute neuromuscular responses in the upper body. J Strength Cond Res. 2010;24(11):2996–3007.
- MacDougall JD, Ray S, Sale DG, et al. Muscle substrate utilization and lactate production. Can J Appl Physiol. 1999;24(3): 209–15.
- Tamaki T, Uchiyama S, Tamura T, et al. Changes in muscle oxygenation during weight-lifting exercise. Eur J Appl Physiol Occup Physiol. 1994;68(6):465–9.
- Suga T, Okita K, Morita N, Yokota T, et al. Dose effect on intramuscular metabolic stress during low-intensity resistance exercise with blood flow restriction. J Appl Physiol. 2010; 108(6):1563–7.
- Fry CS, Glynn EL, Drummond MJ, et al. Blood flow restriction exercise stimulates mTORC1 signaling and muscle protein synthesis in older men. J Appl Physiol. 2010;108(5):1199–209.
- Loenneke JP, Wilson JM, Marin PJ, et al. Low intensity blood flow restriction training: a meta-analysis. Eur J Appl Physiol. 2012;112(5):1849–59.
- Kraemer WJ, Adams K, Cafarelli E, et al. American College of Sports Medicine position stand: progression models in resistance training for healthy adults. Med Sci Sports Exerc. 2002;34(2): 364–80.
- Loenneke JP, Wilson GJ, Wilson JM. A mechanistic approach to blood flow occlusion. Int J Sports Med. 2010;31(1):1–4
- Abe T, Kearns CF, Sato Y. Muscle size and strength are increased following walk training with restricted venous blood flow from the leg muscle, Kaatsu-walk training. J Appl Physiol. 2006;100(5):1460–6.
- Kon M, Ikeda T, Homma T, et al. Effects of low-intensity resistance exercise under acute systemic hypoxia on hormonal responses. J Strength Cond Res. 2012;26(3):611–7.
- Nishimura A, Sugita M, Kato K, et al. Hypoxia increases muscle hypertrophy induced by resistance training. Int J Sports Physiol Perform. 2010;5(4):497–508.
- Goto K, Ishii N, Kizuka T, et al. The impact of metabolic stress on hormonal responses and muscular adaptations. Med Sci Sports Exerc. 2005;37(6):955–63.
- Gordon SE, Kraemer WJ, Vos NH, et al. Effect of acid-base balance on the growth hormone response to acute high-intensity cycle exercise. J Appl Physiol. 1994;76(2):821–9.
- Takarada Y, Nakamura Y, Aruga S, et al. Rapid increase in plasma growth hormone after low-intensity resistance exercise with vascular occlusion. J Appl Physiol. 2000;88(1):61–5
- Henneman E, Somjen G, Carpenter DO. Functional significance of cell size in spinal motoneurons. J Neurophysiol. 1965;28: 560–80.
- Kraemer WJ, Ratamess NA. Fundamentals of resistance training: progression and exercise prescription. Med Sci Sports Exerc. 2004;36(4):674–88.
- Houtman CJ, Stegeman DF, Van Dijk JP, et al. Changes in muscle fiber conduction velocity indicate recruitment of distinct motor unit populations. J Appl Physiol. 2003;95(3):1045–54.
- Sahlin K, Soderlund K, Tonkonogi M, et al. Phosphocreatine content in single fibers of human muscle after sustained submaximal exercise. Am J Physiol. 1997;273(1 Pt 1):C172–8.
- Vollestad NK, Vaage O, Hermansen L. Muscle glycogen depletion patterns in type I and subgroups of type II fibres during prolonged severe exercise in man. Acta Physiol Scand. 1984;122(4):433–41.
- Takarada Y, Takazawa H, Sato Y, et al. Effects of resistance exercise combined with moderate vascular occlusion on muscular function in humans. J Appl Physiol. 2000;88(6):2097–106.
- Ingemann-Hansen T, Halkjaer-Kristensen J, Halskov O. Skeletal muscle phosphagen and lactate concentrations in ischaemic dynamic exercise. Eur J Appl Physiol Occup Physiol. 1981;46(3): 261–70.
- Loenneke JP, Fahs CA, Wilson JM, et al. Blood flow restriction: the metabolite/volume threshold theory. Med Hypotheses. 2011; 77(5):748–52.
- Meyer RA. Does blood flow restriction enhance hypertrophic signaling in skeletal muscle? J Appl Physiol. 2006;100(5): 1443–4.
- Miller KJ, Garland SJ, Ivanova T, et al. Motor-unit behavior in humans during fatiguing arm movements. J Neurophysiol. 1996;75(4):1629–36.
- Debold EP. Recent insights into the molecular basis of muscular fatigue. Med Sci Sports Exerc. 2012;44(8):1440–52.
- Moritani T, Sherman WM, Shibata M, et al. Oxygen availability and motor unit activity in humans. Eur J Appl Physiol Occup Physiol. 1992;64(6):552–6.
- Sundberg CJ. Exercise and training during graded leg ischaemia in healthy man with special reference to effects on skeletal muscle. Acta Physiol Scand Suppl. 1994;615:1–50.
- Yasuda T, Abe T, Sato Y, et al. Muscle fiber cross-sectional area is increased after two weeks of twice daily KAATSU-resistance training. Int J KAATSU Train Res. 2005;1(2):65–70.
- Laurentino GC, Ugrinowitsch C, Roschel H, et al. Strength training with blood flow restriction diminishes myostatin gene expression. Med Sci Sports Exerc. 2012;44(3):406–12.
- Manini TM, Clark BC. Blood flow restricted exercise and skeletal muscle health. Exerc Sport Sci Rev. 2009;37(2):78–85.
- Hansen S, Kvorning T, Kjaer M, et al. The effect of short-term strength training on human skeletal muscle: the importance of physiologically elevated hormone levels. Scand J Med Sci Sports. 2001;11(6):347–54.
- Crewther B, Keogh J, Cronin J, et al. Possible stimuli for strength and power adaptation: acute hormonal responses. Sports Med. 2006;36(3):215–38.
- Kraemer WJ, Ratamess NA. Hormonal responses and adaptations to resistance exercise and training. Sports Med. 2005;35(4): 339–61.
- Haddad F, Adams GR. Inhibition of MAP/ERK kinase prevents IGF-I-induced hypertrophy in rat muscles. J Appl Physiol. 2004;96(1):203–10.
- Stewart CE, Pell JM. Point:Counterpoint: IGF is/is not the major physiological regulator of muscle mass. Point: IGF is the major physiological regulator of muscle mass. J Appl Physiol. 2010;108(6):1820,1; discussion 1823-4; author reply 1832.
- Hameed M, Lange KH, Andersen JL, et al. The effect of recombinant human growth hormone and resistance training on IGF-I mRNA expression in the muscles of elderly men. J Physiol. 2004;555(Pt 1):231–40.
- Kostek MC, Delmonico MJ, Reichel JB, et al. Muscle strength response to strength training is influenced by insulin-like growth factor 1 genotype in older adults. J Appl Physiol. 2005;98(6): 2147–54.
- Philippou A, Papageorgiou E, Bogdanis G, et al. Expression of ИФР-1 isoforms after exercise-induced muscle damage in humans: characterization of the МФР E peptide actions in vitro. In Vivo. 2009;23(4):567–75.
- Goldspink G. Mechanical signals, IGF-I gene splicing, and muscle adaptation. Physiology (Bethesda). 2005;20:232–8.
- Velloso CP, Harridge SD. Insulin-like growth factor-I E peptides: implications for aging skeletal muscle. Scand J Med Sci Sports. 2010;20(1):20–7.
- Velloso CP. Regulation of muscle mass by growth hormone and IGF-I. Br J Pharmacol. 2008;154(3):557–68.
- Timmons JA. Variability in training-induced skeletal muscle adaptation. J Appl Physiol. 2011;110(3):846–53.
- Petrella JK, Kim J, Mayhew DL, et al. Potent myofiber hypertrophy during resistance training in humans is associated with satellite cell-mediated myonuclear addition: a cluster analysis. J Appl Physiol. 2008;104(6):1736–42.
- O’Connor RS, Pavlath GK. Point:counterpoint: satellite cell addition is/is not obligatory for skeletal muscle hypertrophy. J Appl Physiol. 2007;103(3):1099–100.
- McCarthy JJ, Esser KA. Counterpoint: satellite cell addition is not obligatory for skeletal muscle hypertrophy. J Appl Physiol. 2007;103:1100–2.
- Owino V, Yang SY, Goldspink G. Age-related loss of skeletal muscle function and the inability to express the autocrine form of insulin-like growth factor-1 (МФР) in response to mechanical overload. FEBS Lett. 2001;505(2):259–63.
- Sandri M. Signaling in muscle atrophy and hypertrophy. Physiology (Bethesda). 2008;23:160–70. 82. Barton ER. Viral expression of insulin-like growth factor-I isoforms promotes different responses in skeletal muscle. J Appl Physiol. 2006;100(6):1778–84.
- Bamman MM, Petrella JK, Kim JS, et al. Cluster analysis tests the importance of myogenic gene expression during myofiber hypertrophy in humans. J Appl Physiol. 2007;102(6):2232–9.
- Hill M, Wernig A, Goldspink G. Muscle satellite (stem) cell activation during local tissue injury and repair. J Anat. 2003;203(1):89–99.
- Yang SY, Goldspink G. Different roles of the IGF-I ec peptide (МФР) and mature IGF-I in myoblast proliferation and differentiation. FEBS Lett. 2002;522(1–3):156–60.
- Philippou A, Maridaki M, Halapas A, et al. The role of the insulin-like growth factor 1 (ИФР-1) in skeletal muscle physiology. In Vivo. 2007;21(1):45–54.
- Rubin MR, Kraemer WJ, Maresh CM, et al. High-affinity growth hormone binding protein and acute heavy resistance exercise. Med Sci Sports Exerc. 2005;37(3):395–403.
- Kraemer WJ, Aguilera BA, Terada M, et al. Responses of IGF-I to endogenous increases in growth hormone after heavy-resistance exercise. J Appl Physiol. 1995;79(4):1310–5.
- Abe T, Yasuda T, Midorikawa T, et al. Skeletal muscle size and circulating ИФР-1 are increased after two weeks of twice daily KAATSU resistance training. Int J Kaatsu Train Res. 2005;1: 6–12.
- Takano H, Morita T, Iida H, et al. Hemodynamic and hormonal responses to a short-term low-intensity resistance exercise with the reduction of muscle blood flow. Eur J Appl Physiol. 2005;95(1):65–73.
- Fujita S, Abe T, Drummond MJ, et al. Blood flow restriction during low-intensity resistance exercise increases S6K1 phosphorylation and muscle protein synthesis. J Appl Physiol. 2007;103(3):903–10.
- Drummond MJ, Fujita S, Abe T, et al. Human muscle gene expression following resistance exercise and blood flow restriction. Med Sci Sports Exerc. 2008;40(4):691–8.
- Buresh R, Berg K, French J. The effect of resistive exercise rest interval on hormonal response, strength, and hypertrophy with training. J Strength Cond Res. 2009;23(1):62–71.
- Kadi F. Cellular and molecular mechanisms responsible for the action of testosterone on human skeletal muscle: a basis for illegal performance enhancement. Br J Pharmacol. 2008;154(3): 522–8.
- Bhasin S, Woodhouse L, Storer TW. Proof of the effect of testosterone on skeletal muscle. J Endocrinol. 2001;170(1):27–38.
- Zhao W, Pan J, Zhao Z, et al. Testosterone protects against dexamethasone-induced muscle atrophy, protein degradation and MAFbx upregulation. J Steroid Biochem Mol Biol. 2008;110(1–2):125–9.
- Urban RJ, Bodenburg YH, Gilkison C, et al. Testosterone administration to elderly men increases skeletal muscle strength and protein synthesis. Am J Physiol. 1995;269(5 Pt 1):E820–6.
- Vingren JL, Kraemer WJ, Ratamess NA, et al. Testosterone physiology in resistance exercise and training: the up-stream regulatory elements. Sports Med. 2010;40(12):1037–53.
- Sculthorpe N, Solomon AM, Sinanan AC, et al. Androgens affect myogenesis in vitro and increase local ИФР-1 expression. Med Sci Sports Exerc. 2012;44(4):610–5.
- Sinha-Hikim I, Cornford M, Gaytan H, et al. Effects of testosterone supplementation on skeletal muscle fiber hypertrophy and satellite cells in community-dwelling older men. J Clin Endocrinol Metab. 2006;91(8):3024–33.
- Ahtiainen JP, Pakarinen A, Alen M, et al. Muscle hypertrophy, hormonal adaptations and strength development during strength training in strength-trained and untrained men. Eur J Appl Physiol. 2003;89(6):555–63.
- Tremblay MS, Copeland JL, Van Helder W. Effect of training status and exercise mode on endogenous steroid hormones in men. J Appl Physiol. 2004;96(2):531–9.
- Kraemer WJ, Fry AC, Warren BJ, et al. Acute hormonal responses in elite junior weightlifters. Int J Sports Med. 1992;13(2):103–9.
- Loenneke JP, Wilson JM, Pujol TJ, et al. Acute and chronic testosterone response to blood flow restricted exercise. Horm Metab Res. 2011;43(10):669–73.
- Gotshalk LA, Loebel CC, Nindl BC, et al. Hormonal responses of multiset versus single-set heavy-resistance exercise protocols. Can J Appl Physiol. 1997;22(3):244–55.
- Hakkinen K, Pakarinen A. Acute hormonal responses to two different fatiguing heavy-resistance protocols in male athletes. J Appl Physiol. 1993;74(2):882–7.
- Smilios I, Pilianidis T, Karamouzis M, et al. Hormonal responses after various resistance exercise protocols. Med Sci Sports Exerc. 2003;35(4):644–54.
- McCaulley GO, McBride JM, Cormie P, et al. Acute hormonal and neuromuscular responses to hypertrophy, strength and power type resistance exercise. Eur J Appl Physiol. 2009;105(5): 695–704.
- Reeves GV, Kraemer RR, Hollander DB, et al. Comparison of hormone responses following light resistance exercise with partial vascular occlusion and moderately difficult resistance exercise without occlusion. J Appl Physiol. 2006;101(6): 1616–22.
- Viru M, Jansson E, Viru A, et al. Effect of restricted blood flow on exercise-induced hormone changes in healthy men. Eur J Appl Physiol Occup Physiol. 1998;77(6):517–22.
- Vierck J, O’Reilly B, Hossner K, et al. Satellite cell regulation following myotrauma caused by resistance exercise. Cell Biol Int. 2000;24(5):263–72.
- Doessing S, Heinemeier KM, Holm L, et al. Growth hormone stimulates the collagen synthesis in human tendon and skeletal muscle without affecting myofibrillar protein synthesis. J Physiol. 2010;588(Pt 2):341–51.
- Sotiropoulos A, Ohanna M, Kedzia C, et al. Growth hormone promotes skeletal muscle cell fusion independent of insulin-like growth factor 1 up-regulation. Proc Natl Acad Sci USA. 2006;103(19):7315–20.
- Aperghis M, Velloso CP, Hameed M, et al. Serum IGF-I levels and IGF-I gene splicing in muscle of healthy young males receiving rhGH. Growth Horm IGF Res. 2009;19(1):61–7.
- Ehrnborg C, Rosen T. Physiological and pharmacological basis for the ergogenic effects of growth hormone in elite sports. Asian J Androl. 2008;10(3):373–83.
- Kraemer WJ, Dunn-Lewis C, Comstock BA, et al. Growth hormone, exercise, and athletic performance: a continued evolution of complexity. Curr Sports Med Rep. 2010;9(4):242–52.
- Phillips SM. Physiologic and molecular bases of muscle hypertrophy and atrophy: impact of resistance exercise on human skeletal muscle (protein and exercise dose effects). Appl Physiol Nutr Metab. 2009;34(3):403–10.
- West DW, Phillips SM. Anabolic processes in human skeletal muscle: restoring the identities of growth hormone and testosterone. Phys Sportsmed. 2010;38(3):97–104.
- Lange KH, Andersen JL, Beyer N, et al. GH administration changes myosin heavy chain isoforms in skeletal muscle but does not augment muscle strength or hypertrophy, either alone or combined with resistance exercise training in healthy elderly men. J Clin Endocrinol Metab. 2002;87(2):513–23.
- Yarasheski KE, Campbell JA, Smith K, et al. Effect of growth hormone and resistance exercise on muscle growth in young men. Am J Physiol. 1992;262(3 Pt 1):E261–7.
- Yarasheski KE, Zachwieja JJ, Campbell JA, et al. Effect of growth hormone and resistance exercise on muscle growth and strength in older men. Am J Physiol. 1995;268(2 Pt 1):E268–76.
- Nindl BC, Hymer WC, Deaver DR, et al. Growth hormone pulsatility profile characteristics following acute heavy resistance exercise. J Appl Physiol. 2001;91(1):163–72.
- West DW, Kujbida GW, Moore DR, et al. Resistance exercise induced increases in putative anabolic hormones do not enhance muscle protein synthesis or intracellular signalling in young men. J Physiol. 2009;587(Pt 21):5239–47.
- Coffey VG, Shield A, Canny BJ, et al. Interaction of contractile activity and training history on mRNA abundance in skeletal muscle from trained athletes. Am J Physiol Endocrinol Metab. 2006;290(5):E849–55.
- Madarame H, Neya M, Ochi E, et al. Cross-transfer effects of resistance training with blood flow restriction. Med Sci Sports Exerc. 2008;40(2):258–63.
- West DW, Burd NA, Tang JE, et al. Elevations in ostensibly anabolic hormones with resistance exercise enhance neither training-induced muscle hypertrophy nor strength of the elbow flexors. J Appl Physiol. 2010;108(1):60–7.
- Ronnestad BR, Nygaard H, Raastad T. Physiological elevation of endogenous hormones results in superior strength training adaptation. Eur J Appl Physiol. 2011;111(9):2249–59.
- Nielsen AR, Pedersen BK. The biological roles of exercise induced cytokines: IL-6, IL-8, and IL-15. Appl Physiol Nutr Metab. 2007;32(5):833–9.
- Quinn LS. Interleukin-15: a muscle-derived cytokine regulating fat-to-lean body composition. J Anim Sci. 2008;86(14 Suppl.): E75–83.
- Serrano AL, Baeza-Raja B, Perdiguero E, et al. Interleukin-6 is an essential regulator of satellite cell-mediated skeletal muscle hypertrophy. Cell Metab. 2008;7(1):33–44.
- Pedersen BK, Edward F. Adolph distinguished lecture: muscle as an endocrine organ: IL-6 and other myokines. J Appl Physiol. 2009;107(4):1006–14.
- Febbraio MA, Pedersen BK. Contraction-induced myokine production and release: is skeletal muscle an endocrine organ? Exerc Sport Sci Rev. 2005;33(3):114–9.
- Fujita T, Brechue WF, Kurita K, et al. Increased muscle volume and strength following six days of low-intensity resistance training with restricted muscle blood flow. Int J Kaatsu Train Res. 2008;4:1–8.
- Abe T, Beekley MD, Hinata S, et al. Day-to-day change in muscle strength and MRI-measured skeletal muscle size during 7 days KAATSU resistance training: a case study. Int J Kaatsu Train Res. 2005;1:71–6.
- Roth SM, Walsh S. Myostatin: a therapeutic target for skeletal muscle wasting. Curr Opin Clin Nutr Metab Care. 2004;7(3): 259–63.
- Kawada S, Ishii N. Skeletal muscle hypertrophy after chronic restriction of venous blood flow in rats. Med Sci Sports Exerc. 2005;37(7):1144–50.
- Manini TM, Vincent KR, Leeuwenburgh CL, et al. Myogenic and proteolytic mRNA expression following blood flow restricted exercise. Acta Physiol (Oxf). 2011;201(2):255–63.
- Farooqui T. Iron-induced oxidative stress modulates olfactory learning and memory in honeybees. Behav Neurosci. 2008; 122(2):433–47.
- Alessio HM, Hagerman AE, Fulkerson BK, et al. Generation of reactive oxygen species after exhaustive aerobic and isometric exercise. Med Sci Sports Exerc. 2000;32(9):1576–81.
- Powers SK, Talbert EE, Adhihetty PJ. Reactive oxygen and nitrogen species as intracellular signals in skeletal muscle. J Physiol. 2011;589(Pt 9):2129–38.
- Jackson MJ. Reactive oxygen species and redox-regulation of skeletal muscle adaptations to exercise. Philos Trans R Soc Lond B Biol Sci. 2005;360(1464):2285–91.
- Simpson PJ, Lucchesi BR. Free radicals and myocardial ischemia and reperfusion injury. J Lab Clin Med. 1987;110(1):13–30.
- Fulle S, Protasi F, Di Tano G, et al. The contribution of reactive oxygen species to sarcopenia and muscle ageing. Exp Gerontol. 2004;39(1):17–24.
- Jackson MJ. Free radicals generated by contracting muscle: by-products of metabolism or key regulators of muscle function? Free Radic Biol Med. 2008;44(2):132–41.
- Gomez-Cabrera MC, Domenech E, Vina J. Moderate exercise is an antioxidant: upregulation of antioxidant genes by training. Free Radic Biol Med. 2008;44(2):126–31.
- Ji LL, Gomez-Cabrera MC, Vina J. Exercise and hormesis: activation of cellular antioxidant signaling pathway. Ann N Y Acad Sci. 2006; 1067:425–35.
- Thannickal VJ, Fanburg BL. Reactive oxygen species in cell signaling. Am J Physiol Lung Cell Mol Physiol. 2000;279(6): L1005–28.
- Suzuki YJ, Ford GD. Redox regulation of signal transduction in cardiac and smooth muscle. J Mol Cell Cardiol. 1999;31(2): 345–53.
- Hornberger TA, McLoughlin TJ, Leszczynski JK, et al. Selenoprotein-deficient transgenic mice exhibit enhanced exerciseinduced muscle growth. J Nutr. 2003;133(10):3091–7.
- Kefaloyianni E, Gaitanaki C, Beis I. ERK1/2 and p38-MAPK signalling pathways, through MSK1, are involved in NF-kappaB transactivation during oxidative stress in skeletal myoblasts. Cell Signal. 2006;18(12):2238–51.
- Tappia PS, Dent MR, Dhalla NS. Oxidative stress and redox regulation of phospholipase D in myocardial disease. Free Radic Biol Med. 2006;41(3):349–61.
- Handayaningsih A, Iguchi G, Fukuoka H, et al. Reactive oxygen species play an essential role in IGF-I signaling and IGF-Iinduced myocyte hypertrophy in C2C12 myocytes. Endocrinology. 2011;152(3):912–21.
- Korthuis RJ, Granger DN, Townsley MI, et al. The role of oxygen-derived free radicals in ischemia-induced increases in canine skeletal muscle vascular permeability. Circ Res. 1985;57(4): 599–609.
- Clanton TL. Hypoxia-induced reactive oxygen species formation in skeletal muscle. J Appl Physiol. 2007;102(6):2379–88.
- Goldfarb AH, Garten RS, Chee PD, et al. Resistance exercise effects on blood glutathione status and plasma protein carbonyls: influence of partial vascular occlusion. Eur J Appl Physiol. 2008;104(5):813–9.
- Smith LW, Smith JD, Criswell DS. Involvement of nitric oxide synthase in skeletal muscle adaptation to chronic overload. J Appl Physiol. 2002;92(5):2005–11.
- Sellman JE, DeRuisseau KC, Betters JL, et al. In vivo inhibition of nitric oxide synthase impairs upregulation of contractile protein mRNA in overloaded plantaris muscle. J Appl Physiol. 2006;100(1):258–65.
- Anderson JE. A role for nitric oxide in muscle repair: nitric oxide-mediated activation of muscle satellite cells. Mol Biol Cell. 2000;11(5):1859–74.
- Tatsumi R, Hattori A, Ikeuchi Y, et al. Release of hepatocyte growth factor from mechanically stretched skeletal muscle satellite cells and role of pH and nitric oxide. Mol Biol Cell. 2002;13(8):2909–18.
- Kiang JG, Tsokos GC. Heat shock protein 70 kDa: molecular biology, biochemistry, and physiology. Pharmacol Ther. 1998; 80(2):183–201.
- Simar D, Malatesta D, Badiou S, et al. Physical activity modulates heat shock protein-72 expression and limits oxidative damage accumulation in a healthy elderly population aged 60 90 years. J Gerontol A Biol Sci Med Sci. 2007;62(12):1413–9.
- Locke M. Heat shock protein accumulation and heat shock transcription factor activation in rat skeletal muscle during compensatory hypertrophy. Acta Physiol (Oxf). 2008; 192(3):403–11.
- Kregel KC. Heat shock proteins: modifying factors in physiological stress responses and acquired thermotolerance. J Appl Physiol. 2002;92(5):2177–86.
- Paulsen G, Hanssen KE, Ronnestad BR, et al. Strength training elevates HSP27, HSP70 and alphaB-crystallin levels in musculi Role of Metabolic Stress in Hypertrophic Adaptations 193 Author’s personal copy vastus lateralis and trapezius. Eur J Appl Physiol. 2012; 112(5):1773–82.
- Morton JP, Kayani AC, McArdle A, et al. The exercise-induced stress response of skeletal muscle, with specific emphasis on humans. Sports Med. 2009;39(8):643–62.
- Haussinger D, Lang F, Gerok W. Regulation of cell function by the cellular hydration state. Am J Physiol. 1994;267(3 Pt 1):E343–55.
- Haussinger D. The role of cellular hydration in the regulation of cell function. Biochem J. 1996;313(Pt 3):697–710.
- Lang F, Busch GL, Ritter M, et al. Functional significance of cell volume regulatory mechanisms. Physiol Rev. 1998;78(1): 247–306.
- Dangott B, Schultz E, Mozdziak PE. Dietary creatine monohydrate supplementation increases satellite cell mitotic activity during compensatory hypertrophy. Int J Sports Med. 2000;21(1): 13–6.
- Lang F. Mechanisms and significance of cell volume regulation. J Am Coll Nutr. 2007;26(5 Suppl.):613S–23S.
- Low SY, Rennie MJ, Taylor PM. Signaling elements involved in amino acid transport responses to altered muscle cell volume. FASEB J. 1997;11(13):1111–7.
- Clarke MS, Feeback DL. Mechanical load induces sarcoplasmic wounding and FGF release in differentiated human skeletal muscle cultures. FASEB J. 1996;10(4):502–9.
- Lambert IH, Hoffmann EK, Pedersen SF. Cell volume regulation: physiology and pathophysiology. Acta Physiol (Oxf). 2008;194(4):255–82.
- Schliess F, Richter L, vom Dahl S, et al. Cell hydration and mTOR-dependent signalling. Acta Physiol (Oxf). 2006;187(1–2): 223–9.
- Finkenzeller G, Newsome W, Lang F, et al. Increase of c-jun mRNA upon hypo-osmotic cell swelling of rat hepatoma cells. FEBS Lett. 1994;340(3):163–6.
- Schliess F, Schreiber R, Haussinger D. Activation of extracellular signal-regulated kinases erk-1 and erk-2 by cell swelling in H4IIE hepatoma cells. Biochem J. 1995;309(Pt 1):13–7.
- Sjogaard G. Water and electrolyte fluxes during exercise and their relation to muscle fatigue. Acta Physiol Scand Suppl. 1986; 556:129–36.
- Sjogaard G, Adams RP, Saltin B. Water and ion shifts in skeletal muscle of humans with intense dynamic knee extension. Am J Physiol. 1985;248(2 Pt 2):R190–6.
- Frigeri A, Nicchia GP, Verbavatz JM, et al. Expression of aquaporin-4 in fast-twitch fibers of mammalian skeletal muscle. J Clin Invest. 1998;102(4):695–703.
- Kosek DJ, Kim JS, Petrella JK, et al. Efficacy of 3 days/wk resistance training on myofiber hypertrophy and myogenic mechanisms in young vs. older adults. J Appl Physiol. 2006;101(2):531–44.
- Gundermann DM, Fry CS, Dickinson JM, et al. Reactive hyperemia is not responsible for stimulating muscle protein synthesis following blood flow restriction exercise. J Appl Physiol. 2012.
- MacDougall JD, Ward GR, Sale DG, et al. Biochemical adaptation of human skeletal muscle to heavy resistance training and immobilization. J Appl Physiol. 1977;43(4):700–3.
- Chan ST, Johnson AW, Moore MH, et al. Early weight gain and glycogen-obligated water during nutritional rehabilitation. Hum Nutr Clin Nutr. 1982;36(3):223–32.
- Widegren U, Ryder JW, Zierath JR. Mitogen-activated protein kinase signal transduction in skeletal muscle: effects of exercise and muscle contraction. Acta Physiol Scand. 2001;172(3): 227–38.
- Tanimoto M, Sanada K, Yamamoto K, et al. Effects of wholebody low-intensity resistance training with slow movement and tonic force generation on muscular size and strength in young men. J Strength Cond Res. 2008;22(6):1926–38.
- Mitchell CJ, Churchward-Venne TA, West DD, et al. Resistance exercise load does not determine training-mediated hypertrophic gains in young men. J Appl Physiol. 2012.
- Holm L, Reitelseder S, Pedersen TG, et al. Changes in muscle size and MHC composition in response to resistance exercise with heavy and light loading intensity. J Appl Physiol. 2008; 105(5):1454–61.
- Schoenfeld BJ. Does exercise-induced muscle damage play a role in skeletal muscle hypertrophy? J Strength Cond Res. 2012;26(5):1441–53.
Перевод выполнили магистранты:
- Томилов В.В.
- Аракелян Э.А.
- Яковлев А.
- Аверичев С.Ю.
- Хрипунов А.Ф.
- Горячев А.А.
- Назаров М.С.
- Цырульников М.
- Ильина А.И.
- Чернюк С.А.
- Мадисон М.А.
- Крейнина Д.Д.
- Исаева С.В.
- Чихман Н.В.
- Самсонов С.Н.
- Иваницкий С.
- Алякина М.С.
- Михайловская С.А.
- Левин Д.Ю.
- Мельникова Н.Б.
- Цветков А.С.
- Чубовская Ю.В.
- Леготкин Д.А.
- Кубов К.Н.
- Смирнов Т.Н.
- Чиркова Е.А.
- Чернышова А.А.
- Юров А.С.
Под редакцией А.В.Самсоновой
- Возможные механизмы метаболического стресса в гипертрофии мышц