Расщепление миофибрилл у мыши
Установлено расщепление миофибрилл в мышечных волокнах в двуглавой мышце плеча мыши. Причина – несоответствие ромбической решетки актина в Z-диске и гексагональной решетки М-диска. Также обнаружено, что площадь поперечного сечения миофибрилл может увеличиться в 40 раз во время роста мыши и что поперечные трубчатые системы и саркоплазматический ретикулум увеличиваются примерно с той же скоростью.

Г. Голдспинк
Изменения в поперечно-полосатых мышечных волокнах при сокращении и росте с особым вниманием к расщеплению миофибрилл
Аннотация
Ультраструктурные измерения проводились на двуглавой мышце плеча и камбаловидной мышце мыши, закрепленных при различных состояниях сокращения и растяжения. При длине саркомера от 2,7-2,9 мкм при которой более периферийные нити актина находятся под углом к Z-диску. Это происходит из-за несоответствия между ромбической решеткой актина в Z-диске и гексагональной решеткой в М-диске (рис.1).
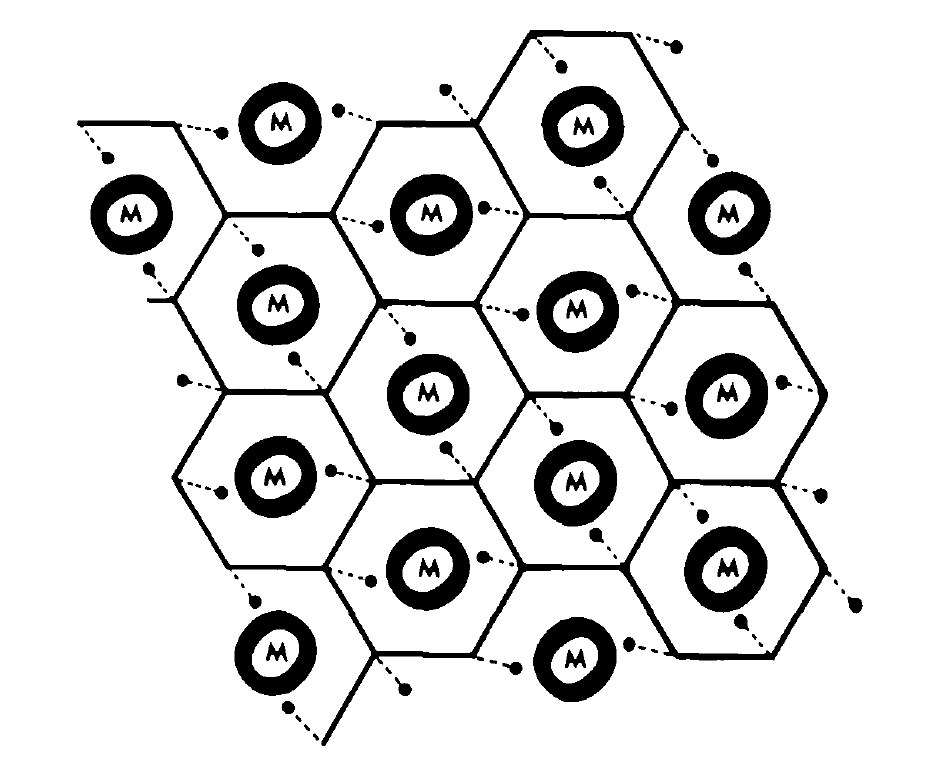
Для идеального преобразования ромбической решетки в гексагональную решетку отношение кристаллической решетки должно быть 1:1,51. Тем не менее, на этой длине саркомера соотношение составляет примерно 1:2,0 (Z:M). При сокращении угол периферических актиновых филаментов остается тем же самым, поскольку расширение решетки М компенсируется частично за счет увеличения расстояния решетки Z-диска и частично за счет изгиба периферийных частей миозина. Когда саркомеры растягиваются за 3,0 мкм миозиновые нити выпрямляются и отношение Z:М уменьшается. Отношение 1:1,51 почти достигается, когда нет перекрытия актина и миозина.
Ультраструктурные измерения были проведены также на двуглавой мышце плеча мышей разных возрастов. Решеточные расстояния для стандартной длины саркомера не изменяются в течение послеродового периода роста. Количество миофибриллярного материала и саркоплазматического ретикулума плюс поперечная трубчатая система были оценены с использованием линейного анализа для мышц в 3 различных стадиях роста. Было обнаружено, что площадь поперечного сечения миофибрилл в индивидуальном мышечном волокне может увеличиться в 40 раз во время роста и что поперечные трубчатые системы и саркоплазматический ретикулум увеличиваются примерно с той же скоростью.
Как в двуглавой мышце плеча, так и в камбаловидной мышце установлено, что актиновые и миозиновые филаменты не состоят из сплошной массы, а делятся на многочисленные отдельные миофибриллы. Деление миофибриллы происходит потому, что миофибриллы расщепляются, как только они достигнут определенного размера.
Доказательства, представленные в этой статье, поддерживает предложение о том, что продольное расщепление миофибрилл происходит из-за разрывов в Z-дисках. Когда напряжение быстро развивается в двух соседних саркомерах, происходит надрыв в центре Z-диска в результате наклонной тяги нитей актина. Это вызывает повреждение некоторых Z-дисков, а затем разрыв распространяется по всему диску с направлением переплетения решетки.
Доказательства механизма включает электронные микрофотографии, показывающие Z-диски, которые, по-видимому, только начинают расщепляться. В этих случаях в центре диска можно видеть отверстие. Описана модель эксперимента, который демонстрирует важность темпов развития напряжения, в результате чего происходит расщепление миофибрилл. Быстрое развитие напряжения производит эффект рывка, который приводит к тому, что повредить Z-диски становится легче. Это может объяснить, почему миофибриллы в быстрых мышцах, как правило, небольшие и отдельные в то время как, в медленных мышцах крупнее и неправильной формы.
Goldspink G. Changes In Striated Muscle Fibres During Contraction And Growth With Particular Reference To Myofibril Splitting // J. Cell Sci. 9, 123-137 (1971)
Abstract
Ultrastructural measurements were carried out on the mouse biceps brachii and soleus muscles fixed at different states of contraction and stretch. At a sarcomere length of 2,7-2,9 µm the more peripheral actin filaments ran slightly obliquely from the Z-disk to the A-band. This is due to a mismatch between the rhombic actin lattice at the Z-disk and the hexagonal lattice at the M-line. For a perfect transformation of a rhombic lattice into a hexagonal lattice the ratio of the lattice spacings has to be 1:1,51. However, at this sarcomere length the ratio is about 1:2,0 (Z:M).
During contraction the angle of the peripheral actin filaments remains approximately the same because the expansion of the M lattice is compensated for, partly by an increase in the Z-lattice spacing and partly by the bowing of the peripheral myosin filaments. When the sarcomeres are stretched beyond 3,0 µm the myosin filaments straighten out and the Z:M ratio decreases. The ratio of 1 :1,51 is almost attained when there is no overlap of the actin and myosin filaments.
Ultrastructural measurements were also carried out on biceps brachii muscles of different ages. The lattice spacings for a standard sarcomere length did not change during the post-natal growth period. The amount of myofibrillar material and sarcoplasmic reticulum plus transverse tubular system were estimated using linear analysis for muscles at 3 different stages of growth. It was found that the myofibrillar cross-sectional area in an individual muscle fibre may increase 40-fold during growth and that the transverse tubular and sarcoplasmic reticulum systems increase at about the same rate.
In both the biceps brachii and the soleus muscles the myosin and actin filaments are not built into a continuous mass but they are divided into numerous discrete myofibrils. Subdivision of the myofibril mass occurs because the myofibrils split once they attain a certain size. The evidence presented in this paper supports the suggestion that the longitudinal splitting of the myofibrils occurs by the ripping of the Z-disks. When tension is rapidly developed by 2 adjacent sarcomeres a stress is produced at the centre of the Z-disk resulting from the oblique pull of the actin filaments.
This causes some of the Z-disk filaments to rip and the rip then extends across the disk with the direction of the weave of the lattice. Evidence for the mechanism includes electron-micrographs showing Z-disks that are apparently just commencing to split; in these cases a hole can be seen in the centre of the disk. A model experiment is described which demonstrates the importance of the rate of tension development in causing myofibril splitting. Rapid tension development produces a snatch effect which causes the Z-disk filaments to break more readily. This may explain why the myofibrils in fast muscles tend to be small and discrete whilst those in slow muscles are larger and more irregular in shape.
REFERENCES
- Ashurst, R. H. (1967). Z line of the flight muscle of belostomatid water bugs. J. molec. Biol. 27, 385-389
- Auber, J. (1969). La myofibrillogenese du muscle strie. I. Insectes. jf. Microscopie 8, 197-232.
- Brandt, P., Lopez, E., Rueben, J. & Grundfest, H. (1967). The relationship between myofilament packing density and sarcomere length in frog striated muscle. J. Cell Biol. 33, 255-263.
- Close, R. (1965). Force: velocity properties of mouse muscles. Nature, bond. 206, 718-719.
- Elliott, G. F., Lowy, J. & Millman, В. M. (1967). Low angle X-ray diffraction studies of living striated muscle during contraction. J. molec. Biol. 25, 31-445.
- Elliott, G. F., Lowy, J. & Worthincton, C. R. (1963). An X-ray and light diffraction study of the filament lattice of striated muscle in the living state and in rigor. J. molec. Biol. 6, 296-306
- Goldspink, G. (1968). Sarcomere length during the post-natal growth of mammalian muscle fibres. J. Cell Sci. 3, 539-548.
- Goldspink, G. (1970). The proliferation of myofibrils during muscle fibre growth. J. Cell Sci.6, 593-603
- Goldspink, G., Larson, R. E. & Davies, R. E. (1970). Thermodynamic efficiency and physiological characteristics of the chick anterior latissimus dorsi muscle. Z. vergl. Physiol. 66, 389-397
- Hess, A. (1961). Structural differences of fast and slow extrafusal muscle fibres and their nerve ending in chickens. J’. Physiol., bond. 157, 221-231.
- Huxley, H. E. (1953). X-ray analysis and the problem of muscle. Proc. R. Soc. В 141, 59-62.
- Huxley, H. E. (1957). The double array of filaments in cross-striated muscle. J. biophys. Cytol. 3, 631-648. Knappeis, G. G. & Carlsen, F. (1963). The ultrastructure of the Z-disc in skeletal muscle. J. Cell Biol. 13, 323-331.
- Kruger, P. (.1950). Untersuchungen an Vogelflugel. Zool. Anz. 145, 460.
- Pilgrim, H. I. & De Оме, К. В. (1955). Intraperitoneal pentobarbital anaesthesia in mice. Expl Surg. 13, 401-403.
- Pringle, J. W. S. (1968). Mechano-chemical transformation in striated muscle. In Aspects of Cell Motility (XXIInd Symp. Soc. exp. Biol.), pp. 67-86. Cambridge University Press.
- Reedy, M. D. (1964). Remarks at a discussion on the physical and chemical basis of muscular contraction. Proc. R. Soc. В 160, 458-460.
- Rowe, R. W. D. & Goldspink, G. (1969). The growth of five different muscles in both sexes of mice. I. Normal mice. J. Anat. 104, 519-530.
- Shear, C. R. & Goldspink, G. (1971). Structural and physiological changes associated with the growth of avian fast and slow muscle. J. Morphol. (In the Press.)
- Smith, C. S. & Guttman, L. (1953). Measurement of internal boundaries in three-dimensional structures by random sectioning. J. Metals 197, Trans. AIME, pp. 81-87.
- Weibel, E. R. (1969). Stereological principles for morphometry in electron microscopic cytology. Int. Rev. Cytol. 26, 235-300.
С уважением, А.В. Самсонова