Повреждение мышц посредством упражнений
Повреждение мышц посредством упражнений часто возникает, если упражнения проводятся в эксцентрическом режиме. Чаще всего эти повреждения включают: «вытекание» Z-полосы и ее «растворение», разрушение A-полосы, распад промежуточной системы филаментов, и некоаксиальность миофибрилл. Механический характер этих повреждений свидетельствует о том, что мышечные волокна повреждаются скорее из-за уровня натяжения волокна, а не абсолютного напряжения, приложенного к волокну. Мы предполагаем, что повреждение, вызванное эксцентрическими сокращениями, происходит во время выполнения упражнений, то есть в течение первых нескольких минут. Структурные повреждения больше в быстрых мышечных волокнах. Выдвинута гипотеза о механизме повреждения, основанном на окислительной способности мышцы, как детерминирующем факторе.
Friden, J. Structural and mechanical basis of exercise-induced muscle injury / J. Frieden, R.L. Lieber //Med. Sci. Sports Exerc., 1992.– Vol. 24.– No. 5.– P. 521-530.
Ж.ФРАЙДЕН, Р.Л.ЛИЕБЕР
СТРУКТУРА И МЕХАНИЧЕСКАЯ ОСНОВА ПОВРЕЖДЕНИЯ МЫШЦ ВЫЗВАННЫХ УПРАЖНЕНИЯМИ
ABSTRACT
В опытах на животных и человеке доказано, что непривычные или эксцентрические упражнения приводят к повреждению сократительной части мышечного волокна или его цитоскелета. Чаще всего эти повреждения включают: «вытекание» Z-полосы и ее «растворение», разрушение A-полосы, распад промежуточной системы филаментов, и некоаксиальность миофибрилл. Механический характер этих повреждений свидетельствует о том, что мышечные волокна повреждаются скорее из-за уровня натяжения волокна, а не абсолютного напряжения, приложенного к волокну. Мы предполагаем, что повреждение, вызванное эксцентрическими сокращениями, происходит во время выполнения упражнений, то есть в течение первых нескольких минут. Структурные повреждения больше в быстрых мышечных волокнах. В заключительной части этой статьи, мы выдвигаем гипотезу о схеме повреждения, основанной на окислительной способности мышцы, как детерминирующем факторе.
Ключевые слова: мышечное волокно, цитоскелет, повреждение миофибрилл, быстрые мышечные волокна
Напряженное упражнение вызывает изменения в гомеостазе мышцы. Хотя ткань мышцы чрезвычайно пластичная (43), разрушительные изменения в тонкой структуре мышцы могут произойти в ответ на необычные требования (17). В опытах на животных (3,28,30,31,37) и человеке (9-13,40) получены структурные повреждения после различных типов упражнения. Описанные повреждения вовлекают: 1) первичное или вторичное разрушение сарколеммы (2,6,21), раздутие или разрушение саркотубулярной системы (2), искажение сократительных компонентов миофибрилл (3,9,11-13,22,31,40), 4) повреждение цитоскелета (10, 5) повреждения внеклеточной матрицы (50).
Такие патологические изменения могут также быть замечены у людей после спринтерского бега или после бега на длинные дистанции (28,41,56), а также после силовой тренировки (14). Так как многие из этих действий содержат большую эксцентрическую составляющую сокращения и потому, что эксцентрическое упражнение, как было установлено – самая разрушительная форма упражнения, много исследователей осуществляли эксцентрические модели сокращения мышцы, чтобы изучить адаптацию к интенсивной физической тренировке (3,12,31,40).
Цель этого обзора состоит в том, чтобы описать реакцию миофибрилл и цитоскелета на высокоинтенсивное упражнение, которое производит повреждение в архитектуре мышцы. Кроме того, мы рассматриваем механику эксцентричных сокращений и выдвигаем гипотезу о механизме, посредством которого вызывается морфологическое повреждение мышечного волокна.
Многие из структурных отклонений после эксцентрического сокращения затрагивают Z-диск. Точная тонкая структура Z-диска полностью не изучена. Однако, так как мы рассматриваем структурные свойства Z-диска в интерпретации миофибриллярных повреждений посредством упражнения, мы чувствуем необходимость дать краткий обзор исследований, посвященных ультраструктуре Z-диска.
Ультраструктура Z-диска
В поперечном сечении, Z-диск появляется как тканная корзина или квадратная решетка. Сообщается, что образцы обмениваются в течение сокращения (29). Чтобы объяснить наблюдаемую ультраструктуру были представлены различные модели (8,15,23,25-27,29,35,47-49,54). Первый структурный анализ Z-диска позвоночных (лягушка m.semitendinosus) был представлен Knappeis и Carlsen (27). Они предположили, что каждая тонкая нить I-полосы с одной стороны Z-диска помещена в центре и равноудалена от четырех тонких филаментов с противоположной стороны диска, и также связана с четырьмя филаментами Z-диска. Franzini-Armstrong и Porter (8) предположили, что Z-диск – это мембрана, к которой прикрепляются концы филаментов I-диска. Reedy (47) описал решетку, состоящую из четырех раскручивающихся жил, подходящих к Z-диску от каждого I-филамента. Kelly (25) предположил, что Z-диск сформирован «жилами», происходящими от одного саркомера, и перекрученными с «жилами» с противоположного саркомера, и возвращающимися, чтобы присоединиться к I-нитям на своей стороне. Каждая I-нить раскололась бы на две «жилы». Rowe (49) также предложил модель, основанную на перекрученных «жилах», хотя он предполагал, что перекрученные «жилы» за счет шпильки присоединились к смежной I-филаменте на своей стороне, но без соединения с «жилами» с противоположной стороны. Kelly и Cahill (26) предложили модель в которой каждая I-нить, дает начало четырем изгибающимся нитям Z-диска, которые простираются на I-филаменты противоположного саркомера. Ullrick с соавт. (54) предположил, что один тонкий филамент, входящий в Z-диск непрерывно связан с тремя изогнутыми Z-филаментами, которые объединяют это с тремя другими тонкими филаментами того же самого саркомера. В более позднем исследовании, Goldstein с соавт. (15) показал, что Z-диск мог бы состоять из концов актиновых филаментов, организованных в комплекс гребенчатой формы, связанных косыми перемычками филаментов. В дополнение ко всем этим разнообразным теориям, нужно также учитывать, что различия в описаниях могли произойти из-за разновидностей и/или различий типов волокон, так же как и технических изменений, типа различных процедур фиксации, толщины сечения и косого направления сечения.
Maruyama и др. (36) считает невозможным представить, как толстые филаменты могли сохранить присутствие в саркомере, не предполагая, что их свободные концы были закреплены к Z-диску некоторой непрерывной упругой структурой. Это также гарантировало бы, что, после сверхрастяжения (то есть, когда наложение актина и миозина исчезает), восстановление мышечными волокнами своей начальной длины и сократительных свойств. Эти функции могли быть приписаны существованию титина, соединенного с толстыми филаментами посредством актиновых филаментов и/или Z-диска (19,36, рис. 1). Согласно этим авторам, возможно, что титиновые филаменты, происходящие из филаментов миозина также могут связаться с другим упругим компонентом, типа линии N2. находящейся близко к Z-диску, где расположен небулин. Другими словами, эти два белка с очень высокой молекулярной массой, очевидно, играют существенную роль в обеспечении осевой непрерывности для производства напряжения покоя, сопротивления растяжению, и обеспечения целостности Z-диска (18,36,44). Кроме того, белки цитоскелета: десмин, виментин, и синемин найдены на периферических Z-дисках миофибрилл, указывая, что эти белки нужно считать интегральными саркомерными компонентами, важными в структуре мышцы и ее механике (45).
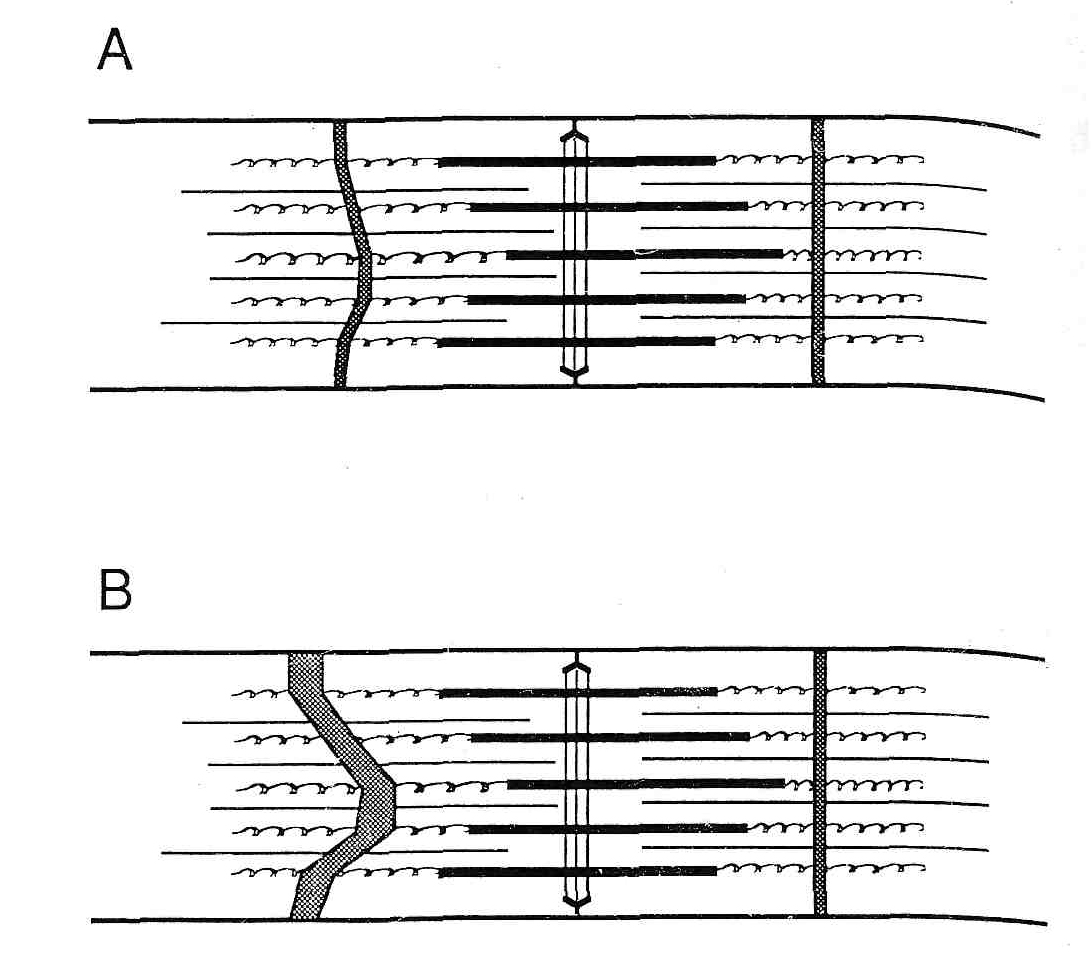
Разрушение миофибрилл после эксцентрического сокращения. Несколько авторов наблюдали изменения в миофибриллах после повторных эксцентричных сокращений (3,11-13,28,40). Friden с соавт. (12) идентифицировали дезорганизацию Z-диска миофибрилл в m. soleus человека через 3 дня после бега по наклонной плоскости. Эти авторы установили характерный вид изменений в сократительном аппарате, включая: расширение, смазывание, или даже общее миофибриллярное разрушение на уровне Z-дисков. Z-полосы смежных миофибрилл не соответствовали друг другу и были загзагообразными (рис. 2A). Дополнительно, некоторые A-полосы в пределах поврежденного саркомера не соответствовали друг другу (рис. 2B) и в некоторых случаях полностью отсутствовали толстые филаменты (9,13). Armstrong с соавт. (3) нашел, что у крыс сразу же после бега по наклонной плоскости, в волокнах медленно разгибающихся мышц были обнаружены разрушения, которые были видны и оптический и электронный микроскоп. Ogilvie с соавт. (42) сообщил о трех типах повреждений: 1) центральные разрушения A-полосы, 2) роспуск Z-линии, и 3) сгущенные волокна. Ogilvie и сотрудники сообщили, что 90 % изменений были связаны с разрушениями A-полосы. Newham с соавт. (40) показал, что, в биопсиях, полученных из m. quadriceps femoris человека, выполняющего эксцентрические сокращения, происходят обширные разрушения саркомеров. Собранные все вместе, эти авторы представили ясное свидетельство драматических структурных отклонений после эксцентрического упражнения.

Биологическое значение разрушения Z-диска, возникающего во время эксцентрических сокращений до настоящего времени неизвестно. Это, однако, является общим нарушением в мышце (5). Fischman с соавт. (7) и Meltzer с соавт. (38) сообщили о «размытом» Z-диске у контрольной группы. Z-дисковое вытекание, кажется, является первичным миофибриллярный ответом на измененные физические и метаболические ситуации. Ясная связь между Z-дисковым вытеканием и высокоинтенсивным физическим упражнением демонстрировалась множеством исследователей (3,12,40). Состав неорганизованного Z-дискового материала полностью не известен, но связывающие белки Z-диска десмин, и спектрин, как было показано посредством электронного микроскопа, могут быть элементами плотного волокнистого материала в областях «размытого» Z-диска (10,52). Являются ли эти полученные данные проявлением саркомерогенезиса, дегенеративных событий, или неустойчивости в обмене миофибриллярных белков не известно.
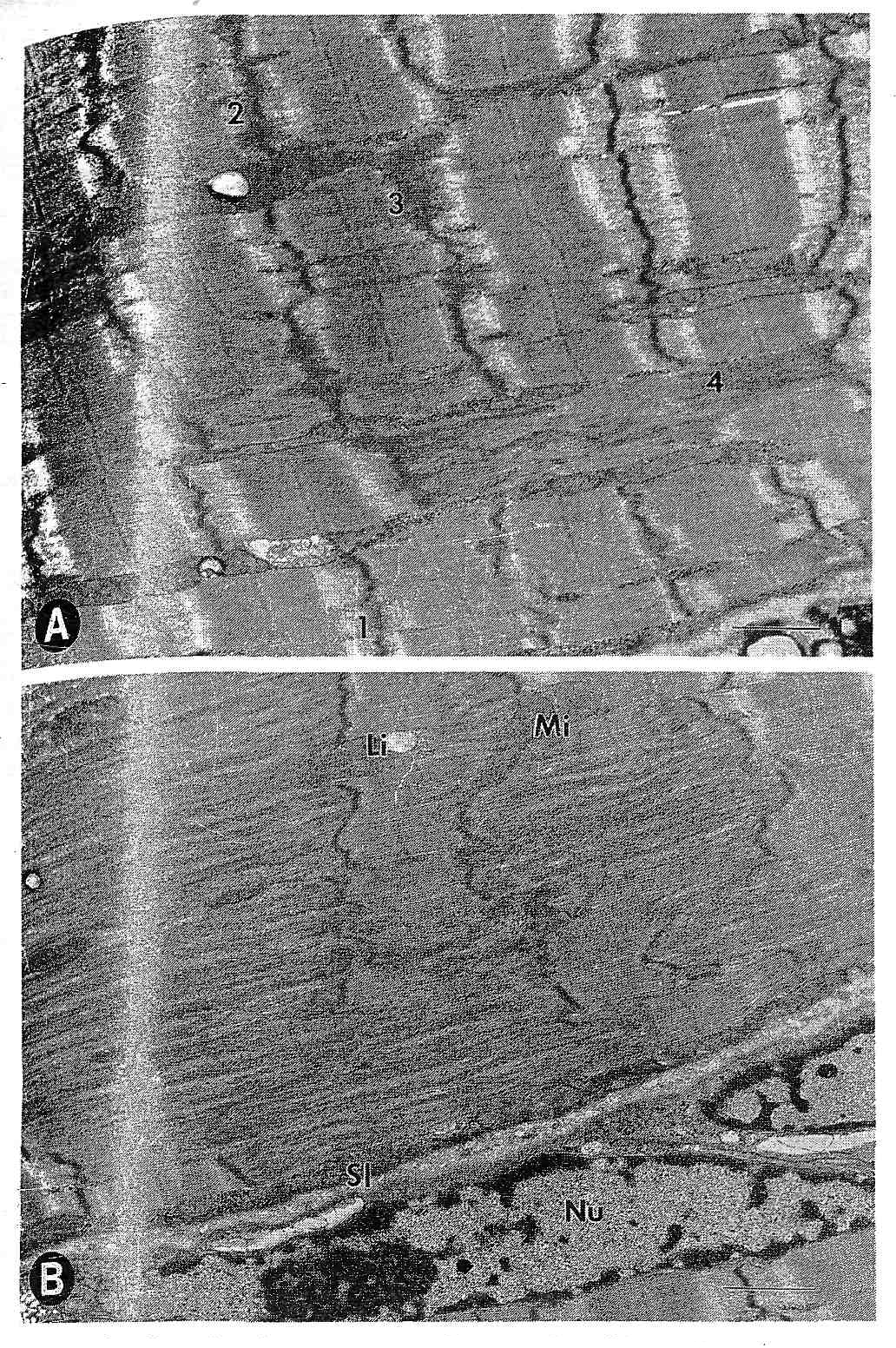
Реакции цитоскелета. Структурная целостность Z-диска и поперечного выравнивания саркомера приписывается существованию филаментных мостиков между Z-дисками и между М -линиями поперек оси волокна (46). Электронная микроскопическая экспертиза ткани мышцы показала наличие филаментов имеющих диаметр 8-12 мкм, которые были названы промежуточными филаментами, на основе их диаметра между тонкими (6 мкм) и толстыми филаментами (16 мкм). Tokuyasu и др. (53) первым показал, что поперечные Z-дисковые связи были составлены из десмина. Они также показали, что десмин связан с митохондриями, ядрами, и сарколеммой. Wang и Ramirez-Митчелл (55) посредством электронной микроскопии продемонстрировали, что в длину ориентируемые промежуточные филаменты начинались на периферии Z-дисков. Такое расположение гарантировало бы свободное движение взаимодействующих толстых и тонких филаментов. Эти авторы заключили, что периферийные продольные промежуточные филаменты могли играть механическую роль в ограничении чрезвычайных изменений длины саркомера.
При использовании иммунофлюоресценции для локализации десмина в мышце vastus lateralis у человека, выполняющего эксцентрические упражнения, мы наблюдали продольные расширения флуоресцентного материала между последовательными Z-дисками в биопсиях через три дня после упражнения (10). Кроме того, эти продольные расширения были беспорядочно распределены всюду по глубине рассечения. Поперечные рассечения укрепили полученные данные, показывая частые сильно флуоресцентные пятна, вкрапленные в регулярные межфибриллярные сети. Эти изменения цитоскелета могут быть вызваны непосредственно высокой напряженностью упражнения, таким образом, представляя повреждение; или они могут представлять вторичный ответ на обширные миофибриллярные повреждения и поэтому представить саркомерогенезис. Последняя интерпретация, таким образом, указывала бы, что увеличенный синтез десмина и перестройка системы цитоскелета, является важной частью в перестройке измененного миофибриллярного материала. Десминовые филаменты, таким образом, действовали бы как механические интеграторы для ремонта саркомеров. Нам нравится эта последняя гипотеза расширенного обмена миофибриллярных и цитоскелетных белков после их деградации. Это – разумное рассмотрение факта, что копии промежуточных филаментов, окружающих Z-диск могут внести свой вклад в дополнение новых саркомеров в пределах поврежденных миофибрилл (55). Увеличение интенсивности окрашивания десмина через три дня после упражнения по сравнению с тем, что было сразу после упражнения, поддерживает это утверждение.
В дополнение к миофибриллярным и цитоскелетным повреждениям, через три дня после упражнения под ультрафиолетом было найдено увеличенное количество липофуксина. Липофуксин вообще расценивается как трудно перевариваемый остаток лизосомальной деградации (51). Факт, что ультраструктурное разрушение достигает пиковых значений через 2-3 дня после упражнения, может указывать на то, что начальное повреждение ухудшается выходом и деятельностью гидролитических ферментов в пределах волокна, далее ухудшая сократительные и цитоскелетные компоненты.
Основываясь на этих наблюдениях, можно предположить, что высокоинтенсивное упражнение может растянуть или разорвать промежуточные филаменты, связывающие Z-диск с Z-диском, а также разрушает дублирующие промежуточные филаменты Z-дискового кольца. Это разрушение молекул белка вызывает разрушение белков Z-дискового кольца, также глобулярных белков и активизирует активность лизосомальных ферментов, вызывая дальнейшую деградацию и в конечном счете разрушение Z-диска. Однако какие обстоятельства приводят к центральному или общему миофибриллярному распаду объяснить невозможно. Чтобы объяснять адаптацию цитоскелета, должно быть предпринято более полное исследование реакции внутрисаркомерного цитоскелета, что позволило бы включить в анализ оценку важности филаментов титина и небулина для того, чтобы предотвратить сверхрастяжение миофибриллы. Если бы, действительно, эти филаменты были бы физически повреждены в результате высокоинтенсивного эксцентрического упражнения, конечно, появилась бы осевая некоаксиальность толстых филаментов (18, рис. 3).
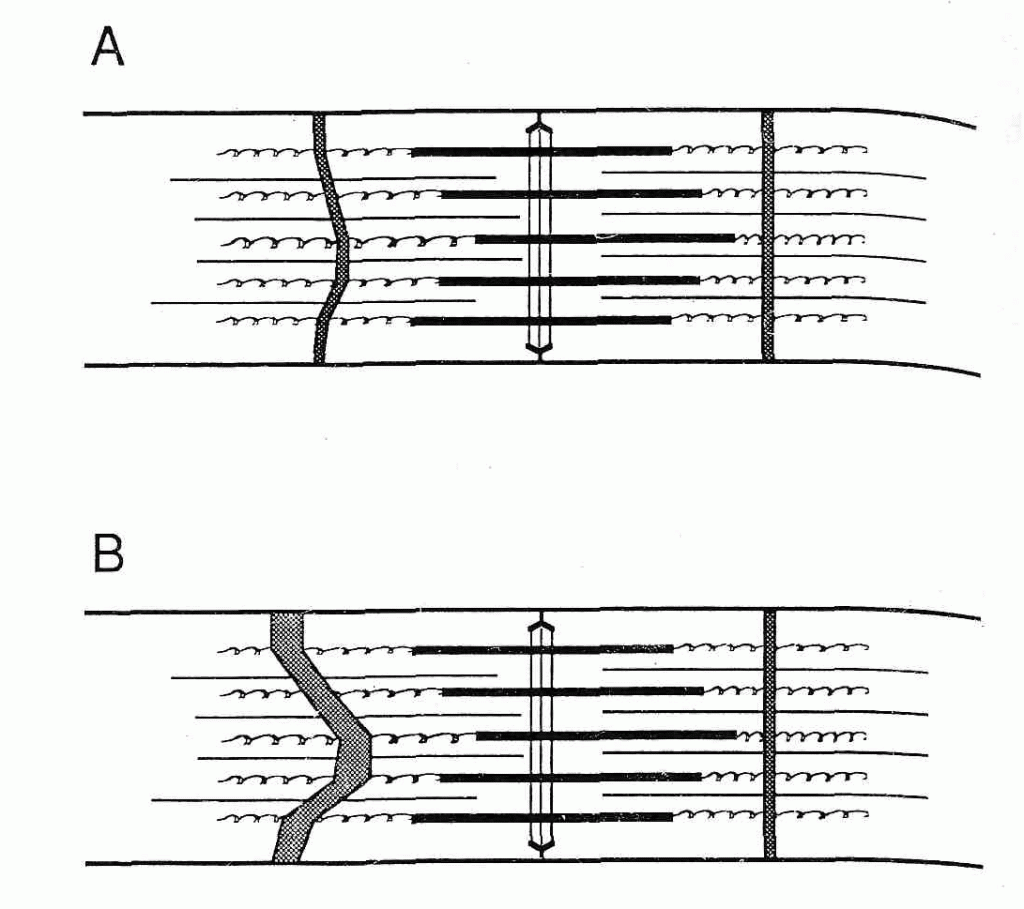
Временные изменения в миофибриллах. Newham с соавт. (40) показал на основе биопсии мышц человека и последующего исследования под микроскопом, что сразу после упражнения 16% мышечных волокон имели легкие повреждения, 16% – более сильные и 8% – очень сильные. Не было, однако, заявлено насколько «немедленно» были взяты эти пробы в минутах. В образцах, взятых через 30 часов после упражнения, увеличилась относительная частота обширных и очень сильных повреждений. Frieden с соавт. (13) показали, что центральные нарушения полос через час после упражнения были обнаружены в 32 % мышечных волокон, через три дня – в 52 %, и через шесть дней – в 12 % мышечных волокон. Таким образом, часть сильно поврежденных мышечных волокон увеличилась через 1-3 дня после упражнения, также, как и общее количество поврежденных волокон. Newham и др. (40) постулировал, что повреждения, замеченные немедленно после упражнения, были предшественниками более сильных повреждений, замеченных в последующих биопсиях. Увеличение общего количества поврежденных мышечных волокон интерпретировалось как повреждение de novo (новое?) после упражнения. Действительно ли это происходит из-за неизбежного процесса ремонта или деятельность мышцы после начального повреждения усиливает повреждение?
Следующее начальное повреждение, связанное с дальнейшей деградацией имеет место в течение следующих часов. Этот процесс, вероятно, инициируется увеличенным количеством внутриклеточного кальция (из-за вызванной утомлением неспособности митохондрий противостоять увеличению кальция), что приводит к активации активизированных кальцием нейтральных протеаз, лизосомных протеаз, и других клеточных процессов, которые связаны с кальцием (1). Интересно, что лаборатория Армстронга недавно предоставила прямое доказательство увеличенной митохондриальной концентрации кальция в крысах, выполняющих длительный бег по наклонной плоскости. Они также показали, что агенты, которые связывали кальций (например, chelating агент, EDTA) уменьшали величину повреждения (6). Armstrong (2) также представил обзор, который подчеркивает критическую роль внутриклеточного регулирования кальция в повреждении мышцы. Мы полагаем, что более серьезное миофибриллярное повреждение, отмечаемое через два и три дня после эксцентрического упражнения, может быть результатом активизированной кальцием, увеличенной протеолитической деятельности ферментов.
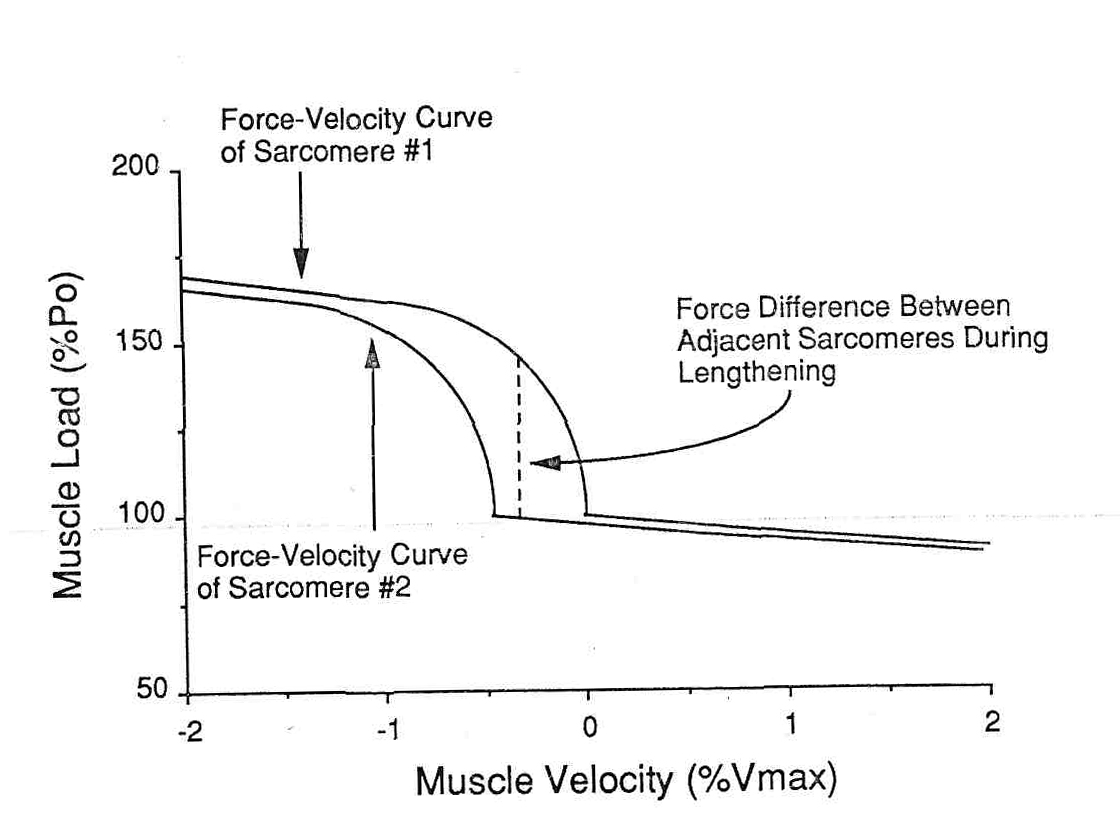
Механическое рассмотрение эксцентрических сокращений. Давно известно, что мышцы, которые удлиняются, могут противодействовать очень большим нагрузкам, и поэтому такие удлиняющие сокращения вызывают повреждение мышцы. Katz (24) объяснил, что механическим основанием этого наблюдения является зависимость «сила-скорость» Он показал, что когда мышце позволяли сокращаться, ее сила уменьшалась почти линейно (по крайней мере в областях низких скоростей) в пределах приблизительно (4%Pо х %Vmax), рис. 4. Таким образом, мышца при сокращении на 5%-ов от Vmax, уменьшает свою силу примерно на 20% от Ро. Однако, для удлинения мышцы, отношения были весьма более сложными. Удлинение мышцы только на 1% от Vmax может увеличить силу на 50% от Ро.
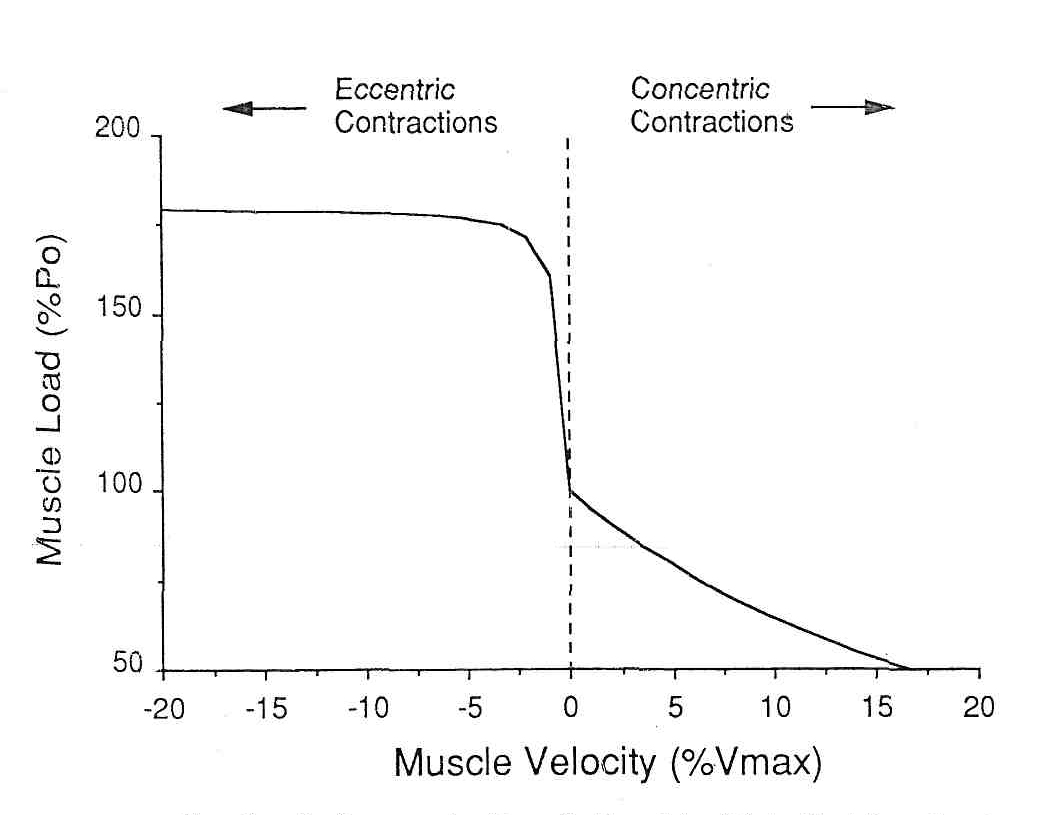
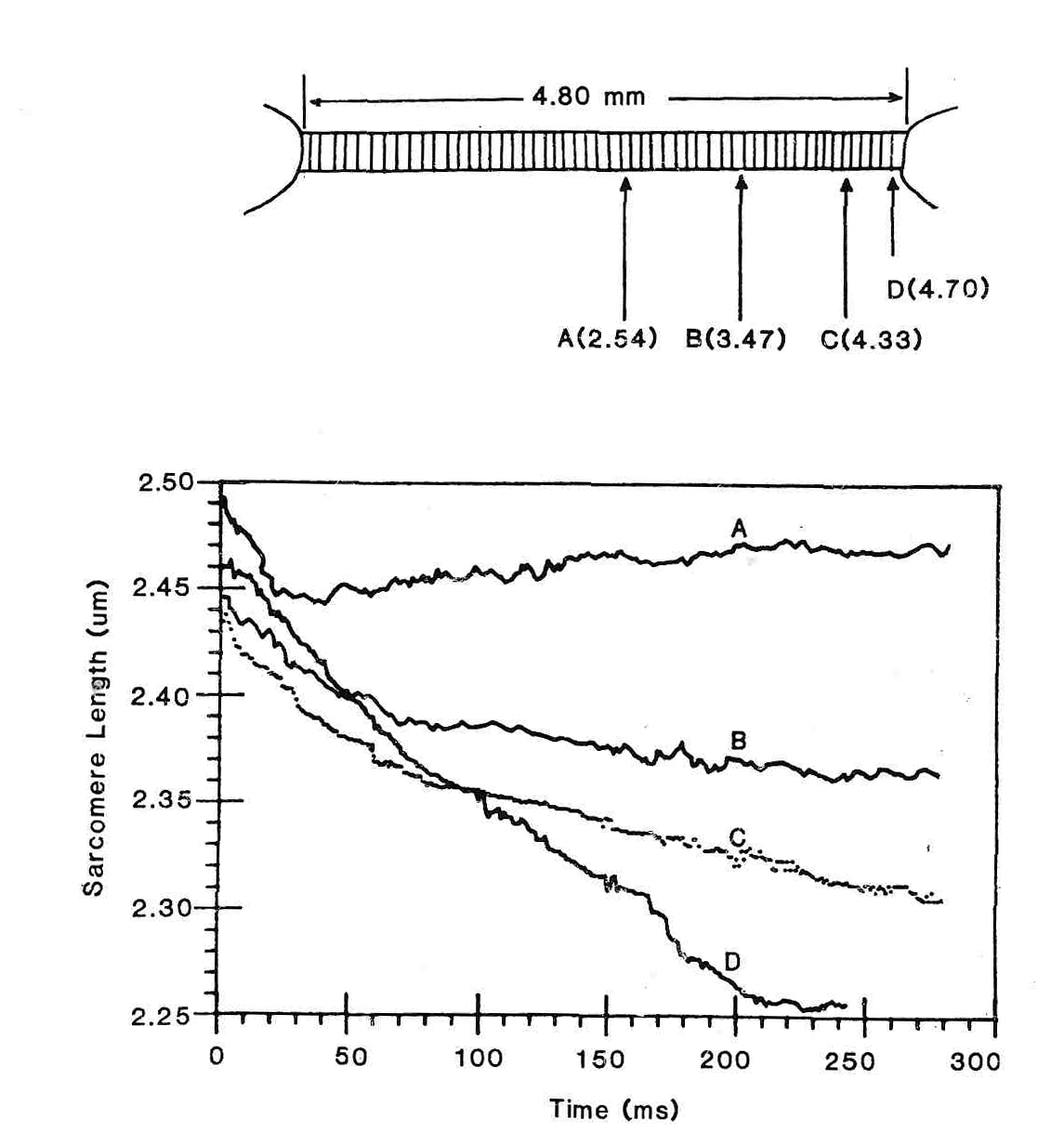
Фактически, неоднородность зависимости «сила-скорость» около нуля приводит к тому, что сила увеличивается приблизительно в 10 раз быстрее при удлинении, чем при такой же скорости сокращения. Эта неоднородность является основанием различий между соседними саркомерами с точки зрения сил, с которыми они взаимодействуют. Вспомните, что длина саркомера относительно длины мышечного волокна может измениться примерно до 1 % (20). В течение сокращений саркомера с одним закрепленным концом установлено, что его скорость для большинства саркомеров, находящихся вдоль длины мышечного волокна варьирует от 1 до 5 % от Vmax (16). Это неравенство длины и скорости может быть ясно замечено на рис.5, который представляет длину саркомера как функцию времени в различных областях изолированного волокна мышцы лягушки (30). Отметьте, что на концах мышечного волокна, саркомеры более короткие и сокращаются с высокой скоростью. К центру мышечного волокна длина саркомеров увеличивается, и скорость сокращения увеличивается. Наконец, в центре волокна, саркомеры относительно длинны и фактически медленно сокращаются в течение изометрического сокращения. Таким образом, каждая смежная популяция саркомеров вдоль волокна имеет немного различную длину и скорость, но производит одно и то же напряжение. Они производят одно и то же напряжение в силу зависимости «сила-длина» мышцы.
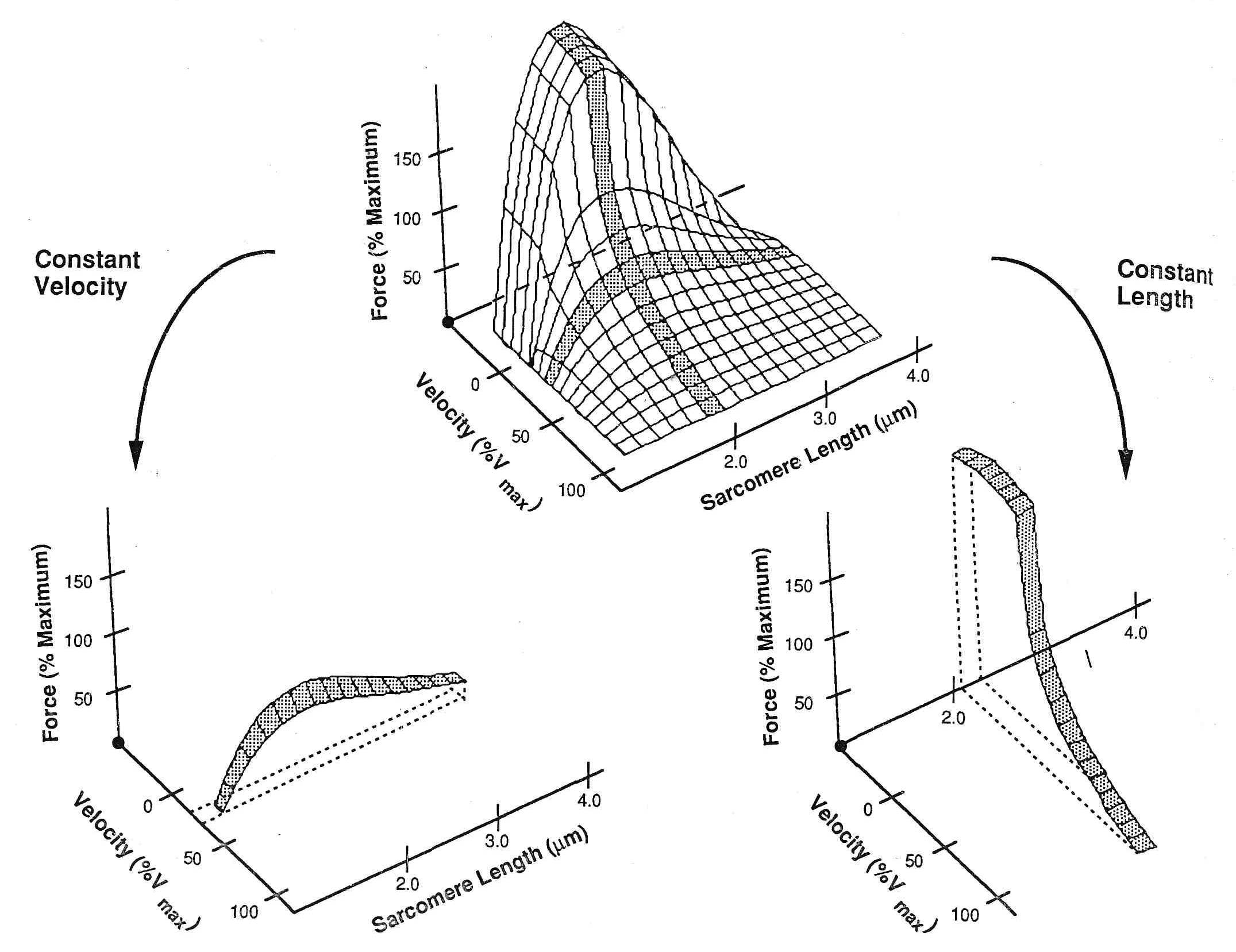
Общую зависимость «длина-сила-скорость» иллюстрирует поверхность (рис.6), в которой длина и/или скорость могут быть различны по почти бесконечному числу комбинаций, чтобы достигнуть специфической силы. Традиционные зависимости «длина-сила» и «сила-скорость» – просто частные случаи этой поверхности, когда любая длина (для зависимости «сила-скорость») или скорость (для зависимости «длина-сила») считается постоянной.
Механическая неустойчивость между смежными саркомерами. Давайте рассмотрим два смежных саркомера, которые имеют немного различные скорости и длину (в пределах физиологического диапазона). Небольшие различия в длине и скорости у укорачивающейся мышцы не несут никакой угрозы, так как отношения кривой «скорость–сила» около нулевой линии не очень круты. Таким образом, для различия Vmax на 0,5 % в течение укорочения, сила, смежных саркомеров изменяется только Pо на 1-2 % (рис. 7). Однако, для смежных саркомеров в течение удлинения, из-за крутизны зависимости «скорость-сила» в смежном саркомере (или даже в смежных областях наложения в пределах саркомера) может измениться больше чем 50%-ым от Pо (рис. 7).
Таким образом, не удивительно, что актиновые филаменты могут испытывать существенно различные силы на своих концах, которые вызовут смещающее напряжение в Z-диске. Возможно, что это смещающее напряжение приводит к «размытию» Z-диска, которое было описано выше. Такой сценарий недавно более подробно рассмотрел Morgan (39), в котором он описывает прогрессивное повреждение смежных саркомеров, поскольку сила волокна превышает их максимальное напряжение растяжения. Если высокое напряжение было бы единственной причиной миофибриллярного разрушения, можно было бы ожидать повреждение, когда пассивное растяжение с высоким напряженным было бы приложено к мышечно-сухожильному соединению. Однако, это, по-видимому, не происходит, так как циклическое пассивное растяжение с напряжением, приближающимся к Pо, изменило максимальное тетаническое напряжение на модели кролика не больше чем 10 % (34). Таким образом, смещение напряжения, а не абсолютное напряжение является более важным в повреждения мышцы. Чтобы проверить гипотезу, что повреждение мышцы непосредственно связано с растяжением мышечного волокна, мы циклически изменяли длину и скорость мышцы tibialis anterior кролика (32). В группе ES (раннее растяжение), мышца был растянута в начале ее активации (рис. 8), величина растяжения составляла 20% от длины волокна, а скорость изменения напряжения составляла 60% в секунду. И величина и степень растяжения были в пределах физиологического диапазона. В группе LS (позднее растяжение), растяжение мышцы было отсрочено на 200 мс, в то время как мышца развивала напряжение. После этого, мышца была растянута так же, как в группе ES. Таким образом, степень растяжения и величина между группами были идентичны. Однако, из-за выбора времени растяжения, пиковая сила, достигнутая в группе LS была почти в два раза больше, чем в группе ES (рис. 8).
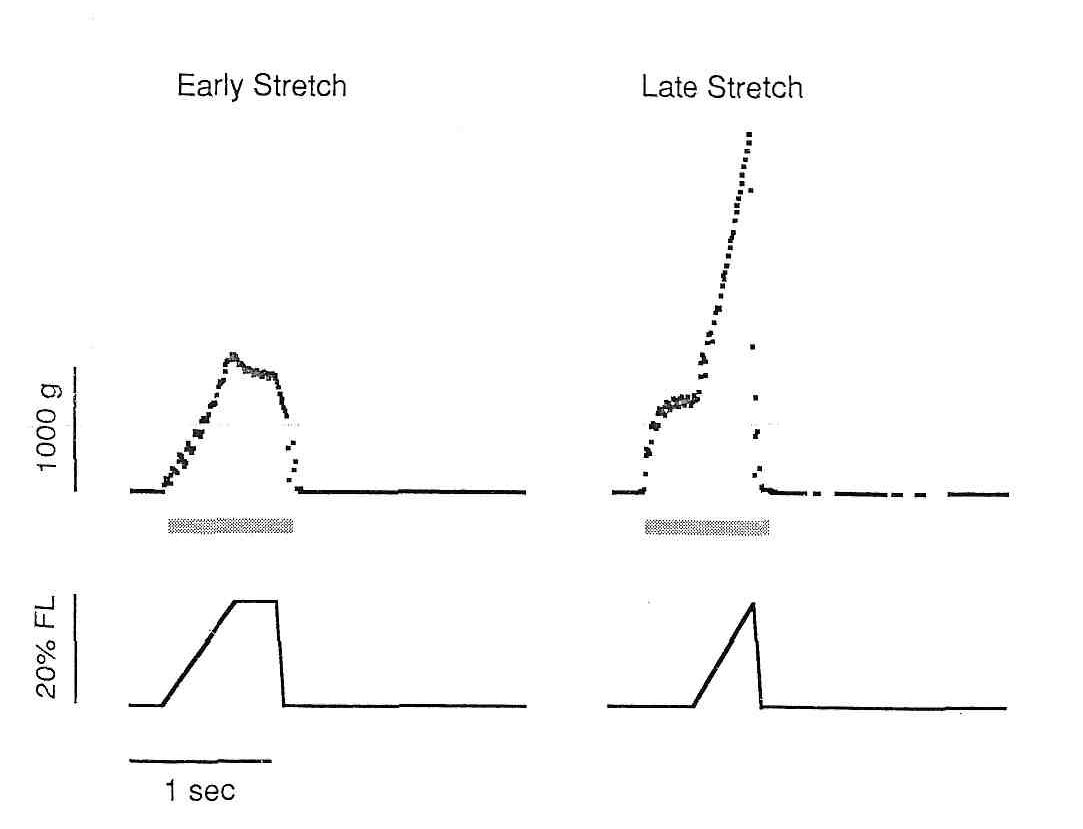
Таким образом, обе группы получили идентичные образцы деформации, но существенно различные напряжения. Интересно, что несмотря на то, что LS группа, дважды стимулировалась для развития полного напряжения в процессе упражнения (30 мин) максимальное тетаническое напряжение после этих двух обработок было почти идентичным (рис. 9). Таким образом, этот эксперимент демонстрирует, что повреждение мышцы, вызванное эксцентричным сокращением, непосредственно не связано с напряжением мышцы. Таким образом, установлено, что напряжение мышцы является высоким в течение эксцентрических сокращений и что повреждение мышцы связано именно с этим типом сокращений, повреждение не обязательно может быть прямой функцией напряжения мышцы. Данные показывают, что саркомер мышцы может иметь физический порог повреждения, который достигается в течение эксцентрического сокращения. В последующем эксперименте, мы варьировали натяжение, приложенное к ТА кролика. У одной группы это натяжение составляло 12.5 % от длины волокна (не от длины мышцы), в то время как у второй группы натяжение составляло 25 % от длины волокна (рис. 9).
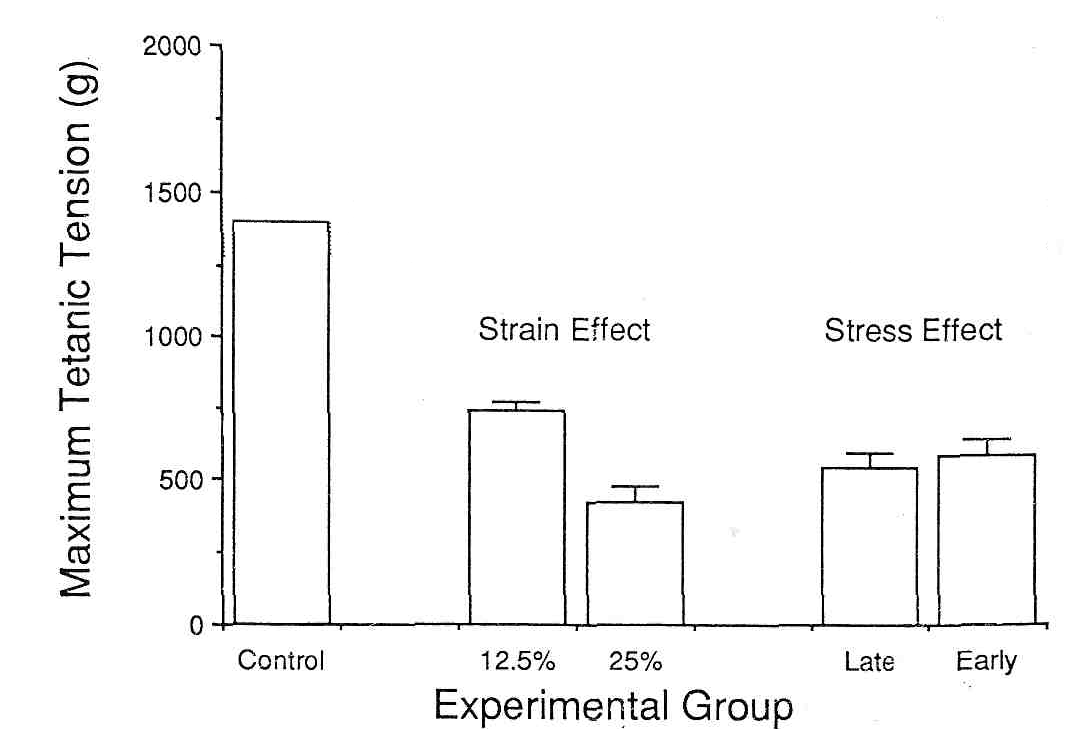
В отличие от вышеупомянутого эксперимента, изменение натяжения имело совсем другие результаты в терминах мышцы Pо. Маленькое натяжение произвело 45%-ое уменьшение Pо, в то время как увеличенное натяжение произвело 65%-ое уменьшение. Если предположить, что повреждение связано не с напряжением, то нужно принять, что натяжение является важным факторов при повреждении мышцы. Напряжение по существу не является повреждающим фактором, так как так как пассивное растяжение не производит никаких ультраструктурных повреждений и минимальных сократительных изменений (34). Только активное растяжение производит повреждение.
Специфика типа волокна и механизм повреждения. В исследовании Friden с соавт. (13), были представлены доказательства, что быстрые волокна повреждаются больше при эксцентрическом сокращении. В том исследовании степень повреждения Z-полосы мышечных волокон IIтипа к I типу было равно 2,8:1 немедленно и 3.0:1 через три дня после упражнения. Мышечные волокна IIВ типа повреждались в 2,5 раза чаще мышечных волокон IIА типа. Нужно, однако, учитывать, что средняя объемная плотность поврежденного материала составляла только 1.6% и 2.4 %, хотя одна треть и половина мышечных волокон были затронуты при выполнении двух биопсий. Данные, свидетельствующие о сильном повреждении быстрых волокон противоречат данным Армстронга с соавт (3), которые при исследовании бега крыс по наклонной плоскости получили данные о сильном повреждении глубоко расположенных волокон первого типа. Однако никакого ультраструктурного исследования типа волокон в том исследовании не было произведено. Это противоречие, возможно связано с несколькими причинами: 1) В исследованиях человека испытуемые могли прекратить упражнение в любое время и в некоторых так и было, когда они ощущали сильный субъективный дискомфорт. Вероятно поэтому в исследованиях на человеке работа в эксцентрическом режиме не приводила к некрозу мышечных волокон. С другой стороны, у животного большой период эксцентрического упражнения конечно вызывал существенные метаболические сдвиги в медленных волокнах 2) в этих исследованиях изучались мышцы с полностью различными функциями. Сопротивление и адаптация к эксцентрическому упражнению может зависеть от различных, к сожалению неизвестных врожденных структурных свойств. 3) возможно, что в глубоком слое, где преобладают медленные мышечные волокна, существуют быстрые мышечные волокна, которые были повреждены. 4) в мышцах большими являются волокна второго типа, а у крыс – волокна первого типа (33). Таким образом, возможно, самые большие волокна наиболее уязвимы для повреждения.
Однако, с ультраструктурной точки зрения, может быть разумно предположить, что более широкие Z-полосы в волокнах I типа менее уязвимы при повторных, высоко интенсивных упражнениях, чем волокна II типа. В морфологическом исследовании бегунов, выполняющих анаэробную работу на тредмиле, мы выполнили полное ультраструктурное изучение поврежденных волокон (11). В этом исследовании была осуществлена специальная фотографическая техника. Эта процедура состояла из проектирования увеличенного изображения неповрежденной части поврежденного волокна через апертуру разреза. Эта апертура после этого перемещалась вдоль фотографической бумаге с постоянной скоростью. Направление движения было параллельно поперечным линиям миофибрилл. Используя эту технику, число и плотность М мостов так же, как ширина Z-полосы могли ясно визуализироваться и использоваться как критерии для ультраструктурной классификации волокон. Через два часа после повторных попыток спринтерского бега в 36% волокон m.vastus lateralis были обнаружены повреждения. Самые заметные изменения были снова связаны с Z-дисковыми отклонениями с центральным и обширным вытеканием. Из поврежденных волокон 80% отклонений были найдены в мышечных волокнах с узкими Z-полосами и имеющих только три М полоски, то есть в волокнах IIB типа. Интересно, биопсия тех же волокон и последующее исследование тех же самых волокон показали истощение гликогена в мышечных волокна I типа и IIB типа, но не в волокнах IIA типа. Однако только в 20 % общего количества мышечных волокон было обнаружено полное истощение гликогена. Это наблюдение может указать существенное метаболическое требование к волокнам IIB типа, которое, в дополнение к эксцентрической нагрузке при беге на длинную дистанцию, увеличивает риск повреждения более тонкого, и возможно более слабого Z-диска волокон IIB типа.
В связи с тем, что недавние исследования на животных показали, что все волокна мышцы, которые имели небольшие повреждения были волокнами FG типа, мы подумали, что окислительная способность мышц могла бы быть причастна к первичным повреждениям мышцы (34). (Отметьте, что метаболическая схема классификации, используемая для мышцы животных – аналогична, но не идентичная базирующейся на активности АТФ-азы схеме классификации мышечных волокон человека). Таким образом, типы SO, FOG, FG аналогичны МВ I типа, IIA типа, IIB типа. Если окислительная способность волокна мышцы, является одним из факторов повреждения волокна, мы могли бы выдвинуть гипотезу о схеме повреждения, которая происходит следующим образом: в ранний период упражнения (в пределах первых 10 минут), наблюдается утомление волокон типа FG. Из-за их неспособности к ресинтезу АТФ, у них наблюдается ригор или высокая жесткость. Последующее растяжение жестких волокон приводит к наблюдаемому разрушению цитоскелета и повреждению миофибрилл. Эта гипотеза поддерживается рядом фактов. Во-первых, она объясняет хорошо известный «защитный» эффект, который связан с тем, что тренировка на выносливость предотвращает повреждения вызванные эксцентрической работой. Тренировка на выносливость, как известно приводит к увеличению окислительной способности мышц и поэтому, волокна типа FG превращаются в волокна типа FOG. Поскольку волокна FOG типа не утомляются и входят в ригор, также, как и волокна FG типа, тренировка на выносливость приводит к меньшим повреждениям, связанным с эксцентрическим сокращением мышц. Понимание этого может быть важным в тренировочных режимах. Эту гипотезу можно экспериментально проверить. Мы предсказываем, что повреждение, вызванное эксцентрическим режимом сокращения мышцы, происходит в первые минуты тренировки. Мы также предсказываем, что утомленная мышца (например, после 20 минут изометрического сокращения) могла бы быть повреждена более значительно, если бы эксцентрическое растяжение было предпринято в конце тренировочного периода. Повреждение не обязательно требовало бы числа растяжений. Теперь остается проверить эти гипотезы.
Второй механизм повреждения, который мог зависеть от окислительной способности волокна, имеет отношение с другими клеточными процессами, которые основаны на окислительном метаболизме. Например, большое уменьшение adenylate мышечного волокна может уменьшить митохондриальную способность противостоять ионам кальция, приводя к активации активизированных кальцием нейтральных протеаз. Интересно, что эти ферменты были недавно вовлечены в процесс дегенерации – регенерации мышечного волокна (4).
РЕЗЮМЕ
Повреждение мышцы, вызванное эксцентрическим сокращением, наблюдается на животных и людях. Хорошо видны повреждения цитоскелета и миофибрилл. Хотя повреждения, связанные с эксцентрическими повреждениями, связаны также с высоким напряжением, возможно большое напряжение само по себе не вызывает повреждений. Активное растяжение, кажется, лучше коррелирует с повреждением. Больше повреждаются быстрые мышечные волокна, имеющие низкую окислительную способность. Это дает возможность предположить, что окислительная способность – важный фактор в повреждении мышцы, вызванном эксцентрическими сокращениями.
REFERENCES
- Armstrong, R. B. Mechanisms of exercise-induced delayed onset muscular soreness: a brief review. Med. Sci. Sports Exerc. i6:529-538, 1984.
- Armstrong, R. B. Initial events in exercise-induced muscular injury. Med. Sci. Sports Exerc. 22:429-435, 1990.
- Armstrong, R. В., R. W. Ogilvie, and J. A. Schwane. Eccentric — exercise-induced injury to rat skeletal muscle. /J. Appl. Physiol. 54:90-93, 1983.
- Badalmente, M. A., L. С Hurst, and A. Stracher. Neuromuscular recovery using calcium protease inhibition after median nerve repair in primates. Proc. Natl. Acad. Sci. 86:5983-5987, 1989.
- Cullen, M. J. and F. L. Mastaglia. Pathological reactions of skeletal muscle. In: Skeletal Muscle Pathology, F. L. Mastaglia and J. Walton (Eds.). New York: Churchill Livingstone, 1982, pp. 114-116.
- Duan, C, M. D. Delp, D. A. Hayes, P. D. Delp, and R. B. Armstrong. Rat skeletal muscle mitochondrial [Ca2+] and injury from downhill walking. J. Appl. Physiol. 68:1241-1251, 1990.
- Fischman, D. A., H. Y. Meltzer, and R. W. Poppei. The ultrastructure of human skeletal muscle: variations from archetypal morphology. In: The Striated Muscle, С M.Pearson and F. K. Mostofi (Eds.). Baltimore: Williams & Wilkins, 1973, pp. 58-76.
- Franzini-Armstrong, С and K. R. Porter. The Z disc of skeletal muscle fibrils. Z. Zellforsch. 61:661-672, 1964.
- Friden, J. Changes in human skeletal muscle induced by long term eccentric exercise. Cell Tissue Res. 236:365-372, 1984.
- Friden, J., U. Kjorell, and L-E. Thornell. Delayed muscle soreness and cytoskeletal alterations: an immunocytological study in man. Int. J. Sports Med. 5:15-18, 1984.
- Friden, J., J. Seger, and B. Ekblom. Sublethal muscle fibre injuries after high-tension anaerobic exercise. Eur. J. Appl. Physiol. 57:360-368, 1988.
- Friden, J., M. Sjostrom, and B. Ekblom. A morphological study of delayed muscle soreness. Experientia 37:506-507, 1981.
- Friden, J., M. Sjostrom, and B. Ekblom. Myofibrillar damage following intense eccentric exercise in man. Int. J. Sports Med. 4:170-176, 1983.
- Giddings, С J., W. B. Neaves, and W. J. Goneya. Muscle fiber necrosis and regeneration induced by prolonged weight lifting in the cat. Anal. Rec. 211:133-141, 1985.
- Goldstein, M. A., J. P. Schroeter, and R. Sass. The Z-band lattice in a slow skeletal muscle../. Muscle Res. CellMotil. 3:333-348, 1982.
- Gordon, A. M., A. F. Huxley, and F. J. Julian. The variation in isometric tension with sarcomere length in vertebrate muscle fibers. J. Physiol. 184:170-192, 1966.
- Hoppeler, H. Exercise-induced ultrastructural changes in skeletal muscle. Int. J. Sports Med. 7:76-92, 1986.
- Horowits, R., E. S. Kempner, M. E. Bisher, and R. J. Podol-sky. A physiological role for titin and nebulin in skeletal muscle. Nature 323:160-164, 1986.
- Horowits, R. and R. J. Podolsky. The positional stability of thick filaments in activated skeletal muscle depends on sarcomere length: evidence for the role of titin filaments. J. Cell Biol. 105:2217-2223, 1987.
- Huxley, A. F. and L. D. Peachey. The maximum length for contraction in vertebrate striated muscle. J. Physiol. 156:150-165, 1961.
- 21- Jenkins, R. R. Free radical chemistry. Sports Med. 5:156-170, 1988.
- Jones, D. A., D. J. Newham, J. M. Round, and S. E. J. Tolfree. Experimental human muscle damage: morphological changes in relation to other indices of damage. J. Physiol. 375:435-448, 1986.
- Katchburian, A„ M. С Burgess, and F. R. Johnson. The effect of tilting ultrathin sections on the image of the Z-disc of skeletal muscle. Experientia 29:1020-1022, 1973.
- Katz, B. The relation between force and speed in muscular contraction. J. Physiol. 96:45-64, 1939.
- Kelly, D. E. Models of muscle Z-band fine structure based on a looping filament configuration. J. Cell Biol. 34:827-840, 1967.
- Kelly, D. E. and M. A. Cahill. Filamentous and matrix components of skeletal muscle Z-disks. Anat. Rec. 172:623-642, 1972.
- Knappeis, G. G. and F. Carlsen. The ultrastructure of the Z disc in skeletal muscle. J. Cell Biol. 13:323-335, 1962.
- Kltpers, H, J. Drukker, P. M. Frederik, P. Geurten, and G. v. Kranenburg. Muscle degeneration after exercise in rats. Int. J. Sports Med. 4:45-51, 1983.
- Landon, D. N. The influence of fixation upon the fine structure of the Z-disc of rat striated muscle. J. Cell Sci. 6:257-276, 1970.
- Lieber, R. L. and R. J. Baskin. Intersarcomere dynamics of single skeletal muscle fibers during fixed-end tetani. J. Gen. Physiol. 82:347-364, 1983.
- Lieber, R. L. and J. Friden. Selective damage of fast glycolytic muscle fibres with eccentric contraction of the rabbit tibialis anterior. Acta Physiol. Scand. 133:587-588, 1988.
- Lieber, R. L. and J. Friden. Muscle stress per se does not cause muscle damage. J. Appl. Physiol, (submitted).
- Lieber, R. L, J. Friden, A. R. Hargens, and E. R. Feringa. Longterm effects of spinal cord transection on fast and slow rat skeletal muscle. II. Morphometric properties. Exp. Neurol. 91:435-448, 1986.
- Lieber, R. L., Т. М. Woodburn, and J. Friden. Muscle damage induced by eccentric contractions of 25% strain. J. Appl. Physiol. 30:86-92, 1991.
- MacDonald, R. D. and A. G. Engel. Observations on organization of Z-disk components and on rod bodies of Z-disk origin. J. Cell Biol. 48:431 -437, 1971.
- Maruyama, К., H. Sawada, S. Kimura, К. Ohashi, H. Higu-chi, and Y. Umazume. Connectin filaments in stretched skinned fibers of frog skeletal muscle./ Cell Biol. 99:1391-1397, 1984.
- McCully, К. К. and J. A. Faulkner. Injury to skeletal muscle fibers of mice following lengthening contractions. /. Appl. Physiol 59:119-126,1985.
- Meltzer, H. Y., R. W. Kuncl, J. Click, and V. Yang. Incidence of Z band streaming and myofibrillar disruptions in skeletal muscle from healthy young people. Neurology 26:853-857, 1976.
- Morgan, D. L. New insights into the behavior of muscle during active lengthening. Biophys. J. 57:209-221, 1990.
- Newham, D. J., G. McPhail, K. R. Mills, and R. H. T. Edwards. Ultrastructural changes after concentric and eccentric contractions of human muscle. /. Neurol. Sci. 61:109-122, 1983.
- Nimmo, M. A. and D. H. Snow. Time course of ultrastructural changes in skeletal muscle after two types of exercise. J. Appl. Physiol. 52:910-913, 1982.
- Ogilvie, R. W, R. В. Armstrong, K. E. Baird, and С L. Bottoms. Lesions in the rat soleus muscle following eccentrically biased exercise. Am. J. Anat. 182:335-346, 1985.
- Pette, D. The Dynamic State of Muscle Fibers. Berlin: Walter de Gruyter & Co., 1990.
- Pierobon-Bormioli, S., R. Betto, and G. SalvIati. The organization of titin (connectin) and nebulin in the sarcomeres: an immunocytolocalization study. /. Muse. Res. CellMotil. 10:446-456, 1989.
- Price, M. G. and E. Lazarides. Expression of intermediate filament-associated proteins paranemin and synemin in chicken development. /. Cell Biol. 97:1860-1874, 1983.
- Price, M. and J. W. Sanger. Intermediate filaments connect Z-disks in adult chicken muscle. J. Exp. Zool. 208:263-269, 1979.
- Reedy, M. K. The structure of actin filaments and the origin of the axial periodicity in the I substance of vertebrate striated muscle. Proc. R. Soc. {Biol) 160:458-460, 1964.
- Rowe, R. W. D. Ultrastructure of the Z line of skeletal muscle fibers. J. Cell Biol. 51:674-685, 1971.
- Rowe, R. W. D. The ultrastrucure of Z disks from white, intermediate, and red fibers of mammalian striated muscles. J. Cell Biol. 57:261-277, 1973.
- Stauber, W. T. Eccentric action of muscles: physiology, injury, and adaptation. Exerc. Sport Sci. Rev. 17:157-185, 1989.
- Tappel, A. L. Lipid peroxidation and fluorescent molecular damage of membranes. In: Pathobiology of Cell Membranes, Vol. 1, B. F. Trump and A. U. Arstila (Eds.). New York: Academic Press, 1975, pp. 145-170.
- Thornell, L-E., A. Eriksson, B. Johansson, et al. Intermediate filament and associated proteins in heart purkinje fibers: a membrane-myofibril anchored cytoskeletal system. Ann. N. Y. Acad.Sci. 455:213-240, 1985.
- Tokuyasu, К. Т., A. H. Dutton, and S. J. Singer. Immunoelectron microscopic studies of desmin (skeletin) localization and intermediate filament organization in chicken skeletal muscle. J. Cell Biol. 96:1727-1735, 198254.
- Ullrick, W. C, P. A. Toselli, J. D. Saide, and W. P. C. The Fine structure of the vertebrate Z-disc. J. Mol. Biol. 115:61 -74,1977.
- Wang, K. and R. Ramirez-Mitchell. A network of transver and longitudinal intermediate filaments is associated with sarcomeres of adult vertebrate skeletal muscle. /J. Cell Biol 96-567 570, 1983.
- Warhol, M., A. Siegel, W. Evans, and L. Silverman. Skeletal
- muscle injury and repair in marathon runners after competition Am. J. Pathol. 118:331-339, 1985.
Перевод А.В.Самсоновой